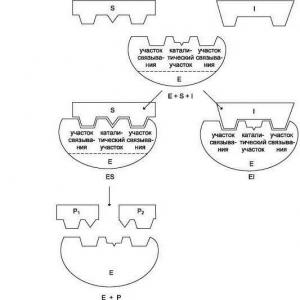
Asetilsalisilik asit sentezi. Asetilsalisilik (2-(asetiloksi)-benzoik) asit
o-Hidroksibenzoik (salisilik) asit, spirea türü (spiraea ulmaria) bitkilerinin çiçeklerinde asetik asit esteri - o-asetilsalisilik asit formunda bulunan doğal bir maddedir. Bu eter, 1874 gibi erken bir tarihte akut eklem romatizmasının tedavisi için tıbbi uygulamaya girdi ve sentetik bir tıbbi madde olarak geçen yüzyılın sonunda aspirin adı altında ticari olarak üretilmeye başlandı ("a" öneki şu anlama geliyordu: bu tıbbi madde spireadan ekstrakte edilmez, kimyasal olarak yapılır). Aspirin 20. yüzyılın ilacı olarak adlandırılıyor ve şu anda dünyada yılda 100 bin tonun üzerinde üretiliyor. Antiinflamatuar, antipiretik ve analjezik özellikleri ile bilinir. Ayrıca kan pıhtılarının oluşumunu önlediği, damar genişletici bir etkiye sahip olduğu ve hatta kalp krizi ve felçlerin önlenmesi ve tedavisi için kullanılmaya başlandığı bulunmuştur. Bu maddenin tıbbi özelliklerinin tam potansiyelinin henüz tükenmediğine inanılmaktadır. Aynı zamanda aspirin, gastrointestinal sistemin iç yüzeyini tahriş ederek kanamaya neden olabilir. Alerjik reaksiyonlar da mümkündür. Vücuttaki aspirin, prostaglandinlerin (özellikle kan pıhtılarının oluşumunu kontrol eden) ve histamin hormonunun (kan damarlarını genişleten ve bağışıklık hücrelerinin iltihaplanma bölgesine akmasına neden olan) sentezini etkiler; ayrıca, müdahale edebilir ağrılı maddelerin biyosentezindeki enflamatuar süreçlerle).
Görünüşte, asetilsalisilik asit beyaz kristal bir toz veya renksiz kristallerdir.
Asetilsalisilik asit suda az çözünür, %96 alkolde kolayca çözünür, eterde çözünür. Yaklaşık 143 0C sıcaklıkta erir.
Alkali çözeltilerde çok, suda az (1:300), etanol (1:7), kloroform (1:17), dietil eter (1:20) içinde çözünür. Salisilik asidin asetik anhidrit ile asetillenmesiyle elde edilir.
Aspirinin sentez şeması, basınç altında ısıtıldığında (5 atmosfere kadar) kuru sodyum fenolat (1) karboksilasyonunu içerir. Sodyum 0-salisilatın (2) izole edilmesinden sonra, HCI'nin etkisiyle serbest salisilik aside (3) dönüştürülür, bu daha sonra asetik anhidrit veya keten ile asetillenir.
Asetilsalisilik asit içeriğinin analizi şu şekilde yapılır: 1.00 g madde, 10 ml %96 alkol içinde çözülmüş, buzlu cam tıpalı bir şişeye konur. 50,0 ml 0,5 M sodyum hidroksit çözeltisi eklenir, şişe kapatılır ve 1 saat inkübe edilir Elde edilen çözelti, indikatör olarak 0,2 ml fenolftalein çözeltisi kullanılarak 0,5 M hidroklorik asit çözeltisi ile titre edilir.
Buna paralel olarak bir kontrol deneyi gerçekleştirilir: 1 ml 0,5 M sodyum hidroksit çözeltisi, 45,04 mg C9H8O4'e karşılık gelir.
Asetilsalisilik asitte, uygun şekilde depolanmazsa safsızlıklar oluşur:

4-hidroksibenzoik asit;

4-hidroksibenzen-1,3-dikarboksilik asit (4-hidroksiizoftalik asit).

2-[hidroksi]benzoik asit.
Ayrıca bakınız
Yakın zamanda ayak bileği ekleminde adduksiyon-inversiyon yaralanması olan hastaların klinik tablosu
Ayak bileği ekleminin bu yaralanmaları olan hastalardaki şikayetler ve klinik tablo, travmatik kuvvetin büyüklüğüne ve eklemin anatomik ve fonksiyonel bozukluklarının doğasına bağlıdır. Birinci derece karakter...
Solunum yolu hastalığı olan 3 ila 7 yaş arası çocuklarda mental durumdaki değişiklikler
Yaşları 3 ila 7 arasında değişen, solunum yolu hastalıklarından muzdarip 15 tıbbi raporu inceledik. Cinsiyete ve hastalık biçimlerine göre yapı Tablo No. 3'te gösterilmiştir. Tablo No. 3. ...
Arka plan
Kardiyovasküler sistem hastalıklarının tedavisine ve önlenmesine büyük bir katkı, yapı ve etki açısından yeni olan bir grup oldukça etkili lipit düşürücü ilaçların yaratılmasıydı - "istatistikler".
100°C'de önceden kurutulmuş 2 g salisilik asit ve 2.8 ml asetik anhidrit küçük bir konik şişeye konur. 2-3 damla konsantre sülfürik asit ekleyin ve balonun içindekileri iyice karıştırın. Karıştırmayı durdurmadan, karışımı 60 °C'de bir su banyosunda 15 dakika ısıtın ve ardından oda sıcaklığına soğumaya bırakın.
Şişeye 30 ml su ekleyin, iyice karıştırın ve çökeltiyi bir Buchner hunisinde süzün. Ham asetilsalisilik asit, eşit hacimlerde asetik asit ve su karışımından yeniden kristalleştirilir, süzülür, filtre üzerinde buzlu su ve ardından toluen ile yıkanır. Bu şekilde elde edilen aspirin 40-60°C'de asetik asit kokusu kaybolana kadar kurutulur. Verim %95. T pl 144 ° С
Sentez Açıklamaları
asilasyon, yani hareketli hidrojen atomlarının asit kalıntıları - asiller - ile değiştirilmesi aminler, fenoller, alkoller ve diğer bileşiklere tabi tutulabilir. Aspirinin sentezi sırasında, salisilik asitteki fenolik hidroksilin hidrojeni, bir asetik asit kalıntısı olan asetil (CH3CO-) ile değiştirilir. Reaksiyon mekanizması aşağıdaki gibi temsil edilebilir:
asetik anhidrit BEN: protonlanmış asetik anhidrit

Bu, asetik anhidritte karbonil karbonda bir nükleofilik sübstitüsyon örneğidir. Elektron çekme etkisinden dolayı orto-salisilik asitteki karboksil grubu, fenolik hidroksilin bazik (ve nükleofilik) özelliklerini zayıflatır. Bu, karışıma bir asit katalizörü (kons. H2S04) eklemeyi gerekli kılar. Fenolün kendisi, asit yokluğunda asetik anhidrit ile açillenir. Karbonil oksijenin protonasyonu katyona yol açar BEN, karbonun elektrofilikliğinin büyük ölçüde arttığı. Bu, nükleofilik saldırıyı ve ara oluşumu kolaylaştırır. III karbonil karbonun geçtiği yer sp 2 - inç sp 3 - durum.
Ürünü seyreltik asetik asitten yeniden kristalleştirirken, hidrolitik ayrışmasını önlemek için çözeltiyi asetilsalisilik asidi çözmek için gerekenden daha uzun süre kaynatmayın. Yeniden kristalleşen ürün süzülür ve çökelti önce az miktarda buzlu su ve ardından soğuk toluen ile yıkanır.
Saf asetilsalisilik asidin erime noktası 144°C'dir. Bununla birlikte, ısıtıldığında ayrışır, bu nedenle gerçek erime noktasının belirlenmesi zordur. Genellikle 129 - 133°C aralığında eriyen bir müstahzar elde edilir.
Kontrol soruları
1. Neden salisilik asit ve asetik anhidrit etkileşiminde, nükleofilik merkez olarak karboksil grubu OH değil de fenolün oksijeni hareket ediyor?
2. Salisilik asidin asile edilmesi neden fenolden daha zordur?
3. Sülfürik asidin salisilik asidin asilasyon reaksiyonunu neden hızlandırdığını açıklayınız?
4. Aspirinin hidroliz reaksiyonunu yazınız. Bu reaksiyon, elde edilen müstahzarın erime noktasının belirlenmesi sonucunu nasıl etkileyebilir? İlacın erime noktasının asetilsalisilik asidin (135 °C) gerçek erime noktasına mümkün olduğunca yakın olmasını sağlamak için ne yapılmalıdır?
5. Asetilsalisilik asidin asidik ortamda hidroliz mekanizmasının şemasını yazınız. Aspirin alkali ortamda hidrolize olur mu?
6. Uzun süre saklanmış aspirinde salisilik asit karışımını saptamak için hangi renk reaksiyonu kullanılabilir? Bu soruyu cevaplamak için fenollerin renk reaksiyonları hakkında bir ders kitabı okumalısınız.
7. Asetilsalisilik asit sentezinde ne gibi önlemler alınmalıdır?
2.1.6. N-Butil asetat
Bir su tutucu ve bir geri akış kondansatörü (Şekil 14) ile donatılmış 100 ml'lik yuvarlak dipli bir şişeye 10 ml buzlu asetik asit, 12 ml koyun. N-bütil alkol, 5 damla kons. sülfürik asit ve "kazan" görevi görecek birkaç küçük porselen parçası. Şişeyi bir kum banyosunda ısıtın. Sıvı yeterince yoğun bir şekilde kaynamalıdır, ancak geri akış kondansatörü "boğulmamalıdır".
Reaksiyon tarafından oluşturulan su, alkol ve ester buharları ile birlikte reaksiyon şişesinden kaçar. Buhar karışımı geri akış kondansatöründe yoğuşur, yoğuşma buradan bir kapana çıkar ve içinde ayrışır. Oluşan ester ve bütil alkolü içeren üst organik katman, şişeye geri döner (akar) ve alt su katmanı kademeli olarak artar.
| Tuzaktaki su miktarının artması durduktan sonra, şişe soğumaya bırakılır ve reaksiyon karışımı, tuzağın içeriği ile birlikte bir ayırma hunisine aktarılır. Alt tabaka ayrılır ve üst tabaka önce su, sonra %5'lik soda solüsyonu ve tekrar su ile yıkanır. Esterler, yıkamalarla kuvvetlice çalkalandığında kararlı emülsiyonlar verir; bundan kaçınmak için ayırma hunisinin sallanmaması, onunla "sekiz" e benzer bir hareket yapılması tavsiye edilir. Yıkanan bütil asetat, kalsine sodyum sülfat ile en az 6 saat süreyle dehidre edilir, ardından fraksiyonel damıtma işlemine tabi tutularak 124-126 °C'lik bir fraksiyon toplanır. %80 verim. T bp 126 °C Bu yöntemle şu elde edilebilir: izobütil alkol - izobütil asetattan, T kip 118 °C, izoamil alkol - izoamil asetattan, T kip 142 °С. |  Pirinç. 14. Suyun azeotropik damıtılmasıyla reaksiyonları gerçekleştirmek için kurulum: 1 - reaksiyon şişesi, 2 - suyu ayırmak için tuzak, 3 - geri akış kondansatörü, 4 - hava veya kum banyosu Pirinç. 14. Suyun azeotropik damıtılmasıyla reaksiyonları gerçekleştirmek için kurulum: 1 - reaksiyon şişesi, 2 - suyu ayırmak için tuzak, 3 - geri akış kondansatörü, 4 - hava veya kum banyosu |
Sentez Açıklamaları
Esterleştirme reaksiyonu tersine çevrilebilir bir süreçtir, bu nedenle karboksilik asidin bir estere daha eksiksiz bir dönüşümünü sağlamak için, elde edilen su reaksiyon karışımından çıkarılır. Bunu yapmak için, suyun reaksiyon kütlesinden formda damıtılarak ayrılma özelliğini kullanın. azeotropik karışım alkol ve ester ile.
Azeotropik bir madde karışımı, belirli bir kaynama noktasına sahip tek bir bileşik olarak kaynar ve damıtır; damıtma ile ayrılamaz. Azeotropik bir karışımın bir örneği, %96 etil alkoldür. Bu azeotropun kaynama noktası 78.17°C'dir. T saf etanol balyaları 78,3 ° C. %100 (“mutlak”) etanol elde etmek için özel yöntemler kullanılmalıdır: susuz tuzlar (CuS04), kalsiyum oksit, metalik magnezyum kullanarak suyu kimyasal olarak bağlayın. Su ayrıca %96 etanole benzen eklenerek ve ardından damıtma yapılarak bir benzen-etanol-su üçlü azeotrop formunda damıtılabilir.
Azeotropik karışımlar, diğerlerine kıyasla daha düşük veya daha yüksek kaynama noktalarına sahip olabilir. T oluşturan bileşenlerin yığınları. Suyu ayırmak için kaynama noktaları minimum olan karışımlar kullanılır. Her uçucu madde çifti azeotropik bir karışım oluşturmaz. Örneğin asetik asit su ile azeotrop oluşturmaz. Ne reaktanların ne de reaksiyon ürününün su ile azeotropik karışımlar oluşturmadığı veya azeotroptaki su-organik bileşik oranının çok düşük olduğu durumlarda (örneğin etil alkol durumunda olduğu gibi), bir solvent oluşturabilen bir çözücü. su ile azeotrop karışımı reaksiyon kütlesine eklenir.su. Bu nedenle, yukarıda açıklanan yönteme göre etil veya propil asetat alındığında, şişeye 35-40 ml kloroform veya karbon tetraklorür eklenir.
92.7°C'de damıtılan su ve bütil alkolün azeotropik bir karışımı (kaynama noktalarıyla karşılaştırın) N-bütanol, su ve asetik asit). %42,5 H2O ve %57,5 alkol içerir. Azeotrop su- N%28,7 H20 ve %71,3 ester içeren -bütil asetat 90,2 °C'de kaynar. Üç bileşenin hepsinin mevcudiyetinde, su-bütanol-bütil asetatın üçlü azeotropik karışımı da damıtılır.
2.2. ELEKTROFİLİK İKAME
AROMATİK ARALIKTA
Bu makale, aspirinin tarlada, yani söğüt kabuğundan nasıl "alınacağı" hakkında konuşacak. Sonuç olarak, baş ağrıları için mükemmel bir ilaç alacaksınız ve.
Eczanelerde satılan aspirin asetilsalisilik asittir. Söğüt kabuğundan asetilsalisilik asit üretimi için hammadde olan salisilik asit içeren bitki çayı elde edebilirsiniz.
Tabletlerde, aktif maddenin içeriği doğal olarak yüksektir ve bu da ilacın etkisini hızlandırır. Söğüt çayında salisilik asit konsantrasyonu düşüktür ve kesinlikle güvenlidir. Ticari olarak satılanların aksine, söğüt kabuğundan elde edilen aspirin çok hafif bir ağrı kesicidir.
Adım 1: Doğru Söğütü Bulmak
Herhangi bir şüpheniz varsa ve belirli bir bitkinin çeşidinden %100 emin değilseniz, onu asla kullanmayın. Hayatı tehdit edici olabilir, hastalığa ve hatta erken ölüme yol açabilir.
4 ana söğüt türü vardır: salkım, siyah, altın saçlı ve beyaz veya gümüş söğüt.

İkincisi, en büyük miktarda salisilik asit içerir. Ayrıca, bulması en kolay olanıdır. Genellikle suya yakın büyür.
Gerçek bir söğüt olduğundan emin olun. Bunu yapmak için önce yapraklara dikkat edin, şöyle görünmeleri gerekir:

Kenarlar aşağı doğru sarılmamış, sivri uçlu, 5-15 cm uzunluğunda, 1-3 cm genişliğinde, havlı, basık gümüşi tüylerle.
İkincisi, kabuk. Eski gövdelerde koyu gri olmalı - kaba uzunlamasına çatlaklı.

Üçüncüsü, bir avuç yaprak alın, biraz öğütün ve kokuyu koklayın. Bu tuhaf tatlı aromayı hatırla. Buna göre kışın bile söğüt belirlemek mümkün olacaktır.
Adım 2: Söğüt ağacının iç kabuğundan bir parça "alın"
Söğütün kimliği doğru bir şekilde belirlendikten sonra, aspirin "çıkarma" işlemine devam edebilirsiniz. Bu amaçlar için ağacın iç kabuğuna ihtiyacınız olacak. Güvenilir bir keskin bıçakla, ağaç kabuğunda dikkatlice bir kare kesmeniz gerekir. Bıçağın yeterince derine indiğinden emin olun. İlgilenilenin dış korteks değil, iç korteks olduğunu unutmayın. Bıçağı bir noktada tutarak kabuğu yavaşça dışarı doğru kaldırın.
Meydanın tüm çevresinde bu ruhla ilerleyin. Çok sert çekme. Bunu yaparsanız, kabuk parçalara ayrılacak ve tüm işler boşa gidecektir. İdeal olarak, bu çok kareyi dışa doğru seçmeniz gerekir.
Kabuğun kısmen beyaz, kısmen pembemsi olduğuna dikkat edin. Pembemsi damarlar tam da bu. ne istiyorsun. Kare parçanın dış kabuğunu yavaşça soyun.
Ağacı kabuğundan mahrum bıraktığınız için endişelenmeyin. Bu küçük yara yeterince çabuk iyileşir ve ağacın genel durumuna zarar vermez. Ancak, söğütleri işlemek için iki kural vardır:
- Yılda iki kez aynı ağaçtan asla kabuk almayın.
- Kabuğu asla gövdenin tüm çevresi boyunca kesmeyin. Yaklaşık avucunuzun büyüklüğünde kare bir parça yeterlidir.
Aksi takdirde, eylemleriniz ağacın durumuna büyük ölçüde zarar verebilir ve hatta muhtemelen onu öldürebilir.
Son Adım: Söğüt Çayı Yapımı
Kabuk parçalarını kahve filtresine koyun. Bir düğüme sarın. Başka bir kahve filtresinin üzerine yerleştirin ve tekrar sarın. Düğümü iplikle sabitleyin. Büyük bir çay poşeti olmalı. Bu arada iki kahve filtresi kullanmanıza gerek yok, bir tane yeterli olacaktır.
Ardından söğüt poşetini kaynar su dolu bir tencereye koyun. Suyun rengini kontrol etmek için ara sıra karıştırın. Yavaş yavaş kırmızımsı kahverengi bir renk alacaktır.
Yaklaşık 20 dakika sonra. Kaynadığı anda uzun süre ateşte tutmayın, birkaç dakika yeterlidir. Çayı istenmeyen safsızlıklardan ve parçacıklardan filtrelemeyi unutmayın. Bu, örneğin bir çay süzgeci, atkı veya gazlı bez kullanılarak yapılabilir. Daha sonra elde edilen içeceğe (isteğe bağlı) biraz şeker ekleyebilir ve içebilirsiniz. İşin garibi, söğüt çayı oldukça hoş bir tada sahip.
Bu aracın yadsınamaz avantajı, %100 doğallığıdır. Dedikleri gibi, katkı maddesi, boya ve koruyucu içermez. Söğüt içeceği, küçük ağrılarla mücadelede mükemmel bir çare. Ancak bağışıklık geliştirebileceğinden çok sık kullanılması önerilmez.
Bir seferde birden fazla bardak içmemeye çalışın. Yeterince ağrınız varsa, bu tedavi muhtemelen işe yaramayacaktır, ancak yine de durumu hafifletebilir. Ve son ipucu: Yemek yapma fırsatınız yoksa (veya sadece tembelseniz :), o zaman en azından sadece söğüt kabuğu çiğneyin. Her şey hiç yoktan çok daha iyidir.
Asit asetilsalisilikum
Kantitatif.
asidimetri yöntemi.
İlacın doğru bir numunesi, öğütülmüş tıpalı bir şişeye konur, su, eter içinde çözülür, birkaç damla karışık indikatör (1 ml metil oranj çözeltisi ve 1 ml metilen mavisi çözeltisi) ilave edilir ve 0,5 ile titre edilir Sulu tabakada leylak rengi görünene kadar M hidroklorik asit çözeltisi. .
Depolamak. İyi kapatılmış bir kapta, ışıktan korunmuş, kuru bir yerde.
Başvuru. Antiromatizmal, antienflamatuar, analjezik, ateş düşürücü.
Sadece yemeklerden sonra uygulayın, süt, mukus için, çünkü. midede keratolitik etkiye sahip serbest salisilik asit salınır (mide duvarlarını eritir, mide kanamasına neden olur → ülser), soda ile reçete edilir. Ayrıca kalp üzerinde toksik etkisi vardır, bu nedenle kafein ile reçete edilir.
Asetik asit salisilik ester
| C 9 H 8 O 4 | M v. 180.16 |
Fiş. Salisilik asit ve asetik anhidritten.
Tanım. Renksiz kristaller veya beyaz kristal toz, kokusuz veya hafif kokulu, hafif asidik tat. İlaç kuru havada stabildir, nemli havada yavaş yavaş asetik ve salisilik asitlerin oluşumu ile hidrolize olur.
çözünürlük. Suda az çözünür, alkolde serbestçe çözünür, kloroformda, eterde, kostik ve karbonik alkali çözeltilerinde çözünür.
Özgünlük.
1) alkali hidroliz preparasyonun ardından, varlığı ferrik klorür ile reaksiyona girerek kanıtlanan salisilik asidin ve asetik asitin asetik-etil ester oluşumunun reaksiyonuyla kanıtlandığı salisilik asidin salınması takip eder. Preparat, bir sodyum hidroksit çözeltisi ile 3 dakika kaynatılır, ardından soğutulur ve seyreltilmiş sülfürik asit ile asitleştirilir; beyaz kristal bir çökelti salınır. Çözelti başka bir test tüpüne boşaltılır ve üzerine alkol ve konsantre sülfürik asit ilave edilir; solüsyon etil asetat kokusuna sahiptir. Çökeltiye birkaç damla ferrik klorür çözeltisi eklenir; mor bir renk belirir.
2) Mark'ın reaktifi ile reaksiyon (porselen tabakta). İlaç porselen bir kaba konur, konsantre sülfürik asit ilave edilir, karıştırılır ve birkaç damla su ilave edilir; asetik asit kokusu var. Daha sonra formalin eklenir; pembe bir renk belirir.
kantitatif.
1) Alkalimetri yöntemi.
İlacın tam ağırlığı, fenolftalein (5-6 damla) ile nötralize edilmiş alkol içinde çözülür ve 8-9°'ye soğutulur. Solüsyon 0,1M sodyum hidroksit solüsyonu ile aynı indikatör ile pembe renk elde edilinceye kadar titre edilir.
Doğrudan titrasyon formülü.
2) Hidroliz sonrası asidimetri yöntemi.
NaOH + HCI \u003d NaCl + H20
Geri titrasyon formülü.
Depolamak. İyi kapatılmış bir kapta.
Başvuru. Antiromatizmal, antienflamatuar, analjezik, ateş düşürücü.
Hazırlıklar. tabletler 0.25; 0,5; karmaşık dozaj formlarının bir parçasıdır.
Ürotropin, karbonatlar ile nemli karışımlar verir.
Kazan Devlet Teknoloji Üniversitesi
bölüm TTXV
ortaokul №38
Araştırma
"Asetilsalisilik asit sentezi ve
özgünlüğünün belirlenmesi
Tamamlayan: Elena Veselova
38 Nolu Okul, 10 "teknolojik sınıf"
Novo - Savinovsky bölgesi, Kazan.
Bilim danışmanı:
Doç. kafe HTOSA Sobachkina T.N.
Kazan 2009.
1. Giriş……………………………………………….3
2. "Aspirin" sentezi……………………………………3
3. Ekipman yıkamalarının analizi…………..4
4. Sonuç……………………………………………………..5
5. Deneysel kısım……………………………….5
6. Hesaplama……………………………………………………..6
giriiş
İlaçların büyük kısmı ve tüm vitaminler karmaşık organik maddelerdir. Biyolojik olarak aktif maddelerin önemli bir kısmı kimyasal sentez yoluyla elde edilir. Son yıllarda yeni ilaçlar, kimyasal ve farmasötik müstahzarların sentezi için yeni yöntemler ortaya çıktı.
Ancak kanıtlanmış teknolojilerin, örneğin aspirin (asetilsalisilik asit) sentezinin saygınlığı, önemi ve ihtiyacı azalmaz.
Aspirin saflaştırılmış salisilik asitten elde edilir. Aspirin üretimindeki ikinci tür hammadde, miktarı farklı olabilen asetik anhidrittir - bir veya iki eşdeğer.
Asetilsalisilik asit elde etmenin iki yöntemi vardır:
Ι yöntemi, bir çözücü olan benzen varlığında bir mol asetik anhidritin kullanılmasıyla karakterize edilir.
ΙΙ yöntemi ile asetik anhidrit asidik bir ortamda çift miktarda alınır.
aspirin sentezi
Aspirin sentezini ikinci yöntemle gerçekleştirdik.
Reaksiyon aspirin üretir:
OH OSOSN3
2(CH3CO)2O + (CH3CO)2O + CH3COOH
UNSD UNSD
T pl.\u003d 136 - 137˚ C
Her iki yöntem de yan ürünlerin oluşumu ile karakterize edilir:
"diplosal" "acesal"
Ancak teknolojinin gözetilmesiyle dışlanabilirler.
Herhangi bir ilacın sentezindeki bir sonraki ana görev, ilaçların analitik kontrolüdür. Sentez sırasındaki bu kontrol, büyük ilgiyi hak eder ve elde edilen ilaç substratı miktarının sağlanması amaçlanır.
Böylece "aspirin" sentezledikten sonra ilacın orijinalliği ve kantitatif tespiti için analizler yaptık. Gerçeklik: Alkali ile kaynatıp çözeltiyi sülfürik asitle asitlendirdiğimizde beyaz bir çökelti oluştuğunu gözlemledik; alkol solüsyonunun keskin bir eterik kokusu vardır. Ferrik klorür solüsyonunda, formalin ilavesiyle parlak mor bir renklenme, pembe bir renklenme.
Aspirin miktarı ölçüldü.
Aldığımız aspirin ile eczanedeki aspirini karşılaştırdık, orijinallik ve kantitatif belirleme açısından aynı sonuçları aldık.
Ekipman yıkama analizlerinin yapılması
İlaç üretiminin özelliği, nitratlayıcılar gibi çok amaçlı ekipmanların kullanılmasıdır.
Bu bağlamda, bir sonraki ana görev, ekipman temizleme prosedürlerinin etkinliğini doğrulamaktır. Bu, ortaya çıkan ürünlerin çapraz kontaminasyonunu önlemek için yapılmalıdır.
Bu amaçla, en son işlenen ilaca dahil olan ana maddenin varlığı için ekipmanın çalışma yüzeylerinden alınan sürüntülerin analizi kullanılır.
Bu maddenin sifonunda% 0,1'den fazla olmamalıdır.
Araştırma yöntemleri çözeltilerin analizine dayandığından, yıkamalarda eser miktarların kantitatif tayininde çözücü önemli bir rol oynar.
Bu nedenle, başlangıçta ortaya çıkan "aspirin" için çözücüler seçtik.
çözücüler
Analiz için çözücüler, dozaj formuna göre (tabletler, kapsüller, tozlar, vb.) seçilir.
Tabloda sunulan tüm çözücüler arasında aspirin çalışmalarında distile su, etil alkol ve sodyum hidroksit kullanılabilir.
Eriklerde aspirin analizi için en evrensel yöntemlerin spektrofotomi ve fotokolorimetri olduğu literatürden bilinmektedir.
fotometri - Analiz edilen maddelerin reaktivitesi, bazında renkli bileşikler elde etmeyi mümkün kılıyorsa kullanılabilir.
Spektrofotometrik yöntem - fotokolorimetriye göre bir avantajı vardır, çünkü bunları renkli bileşiklere dönüştürmek için reaksiyonlar gerektirmez, ancak spektrumun ultraviyole bölgesinde yoğun ışık absorpsiyonu meydana gelir.
Çözüm:
1. Asetilsalisilik asidin sentezi ve analizine ilişkin literatür materyali incelenmiştir.
2. Aspirin sentezi yapıldı. Verim, erime noktası belirlenir.
3. Aspirinin orijinalliği ve kantitatif içeriği belirlendi.
4. Sentezlenen ve eczane aspirini ile ilgili verilerin karşılaştırılması yapılmıştır.
5. Ekipman yıkamalarının analizine duyulan ihtiyaç gösterilmiştir.
Deneysel kısım.
Asetilsalisilik asit sentezi.
Şişeye 3,5 g salisilik asit dökülür, 4,5 ml dökülür. Asetik anhidrit, 2-3 damla konsantre sülfürik asit. Karışım 60°C'deki su banyosunda 20-30 dakika karıştırılarak ısıtılır, oda sıcaklığına soğutulur, bir bardak suya dökülür. Ayrılan çökelti süzülür. Tartım için çıktıyı belirleyin.
Verim %97, T pl. 136-137˚С (su, asetik asit).
2. Özgünlük
0,5 g ilaç 5 ml ile 3 dakika kaynatılır. sodyum hidroksit çözeltisi, daha sonra soğutulur ve seyreltik sülfürik asit ile asitleştirilir, beyaz kristalli bir çökelti açığa çıkar. Çözelti başka bir test tüpüne boşaltılır ve üzerine 2 ml eklenir. alkol ve 2 ml. konsantre sülfürik asit, çözelti etil asetat kokusuna sahiptir. Tortuya 1-2 damla ferrik klorür çözeltisi eklenir, mor bir renk görülür.
Porselen kaba 0,2 g ilaç konur, 0,5 ml eklenir. konsantre sülfürik asit, karıştırın ve 1-2 damla su ekleyin, asetik asit kokusu gelir. Daha sonra 1-2 damla formalin ekleyin, pembe bir renk belirir.
3. Kantitatif.
Yaklaşık 0.5 g ilaç (doğru tartılmış) 10 ml'de çözülür. fenolftalein (5-6 damla) ile nötralize edildi ve 8˚ -10˚ alkole soğutuldu. Solüsyon aynı indikatör 0.1 ve sodyum hidroksit solüsyonu ile pembe renk elde edilene kadar titre edilir.
Hesaplama.
maske = 0,6462 gr.
V(NaOH) = 36.7 mi.
T(NaOH) = 0,0038025
MM (NaOH) = 40
T(NaOH)* V*M.M asp
M'asp. =
m'asp. = 0,6281 gr.
m'asp. * 100%
C asp = masp.