Dijabetes melitus tip 2 bez patogeneze gojaznosti. Osnovna istraživanja
Hajde da shvatimo koja je to podmukla dijagnoza?
Uprkos "slatkom" imenu, ovo je ozbiljno hronična bolest endokrini sistem, zbog čega tkiva pacijenta gube osjetljivost na inzulin.
By Međunarodna klasifikacija bolesti (ICD 10) dijabetes melitus tip 2 (nezavisan od insulina) ima šifru E11.
Ova bolest je jedna od najčešće dijagnostikovanih, što podstiče naučnike širom sveta da marljivo proučavaju ovu patologiju.
- Gojaznost, nezdrava ishrana;
- Starost: Stariji ljudi su ranjiviji;
- Stres, užurbani način života;
- Nasljednost;
Šta pacijent treba da uradi da ne bi pogoršao sliku?
Ljudi sa takvom dijagnozom mogu mirno da žive normalnim životom i da budu srećni! Samo morate uvijek paziti na najmanje promjene. Potrebno je često posjećivati ljekara radi praćenja toka bolesti i njenog napredovanja.

Važno pravilo- potrebno je da kreirate pravu dnevnu rutinu. Da biste izbjegli prejedanje ili premalo jedenja, rasporedite svaki obrok, ishranu neka bude umjerena - pridržavati se dijete.
Trebali biste se ograničiti na šećer i masti nebiljnog porijekla. Važno je uvesti fizičku aktivnost u svoj život, ali prije nego to učinite potrebna je konsultacija sa specijalistom!
Doktor će vam detaljno reći zašto je dijabetes tipa 2 opasan, a šta će samo naštetiti i izazvati komplikacije. Česte šetnje svježi zrak biće lep bonus!
Koristan video
Ne može svako zamisliti hitnost problema i 2 vrste. To je zbog brzog porasta broja slučajeva, jer svako, od mladih do starijih, može pasti u ciljnu oblast. Za više detalja pogledajte naš video.
Zaključak
 Od 2014 broj dijabetičara iznosio je 422 miliona. Brojka raste svake minute zbog manje aktivnog načina života ljudi.
Od 2014 broj dijabetičara iznosio je 422 miliona. Brojka raste svake minute zbog manje aktivnog načina života ljudi.
T2DM je veliki problem globalnog zdravlja i svakog čovjeka.
Ako svi prate stanje svojih najmilijih i primjećuju bilo kakve male promjene, čovječanstvo će moći smanjiti broj oboljelih. I tada će doktori rjeđe proglasiti potvrdu bolesti.
49095 0
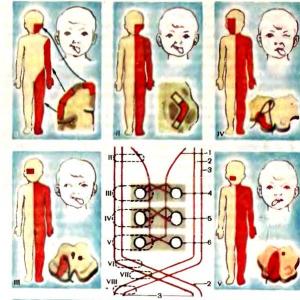
Dijabetes melitus tip 2- kronična bolest koja se manifestira poremećenim metabolizmom ugljikohidrata s razvojem hiperglikemije zbog inzulinske rezistencije i sekretorne disfunkcije β-ćelija, kao i metabolizma lipida s razvojem ateroskleroze. Budući da su glavni uzrok smrti i invaliditeta pacijenata komplikacije sistemske ateroskleroze, T2DM se ponekad naziva kardiovaskularna bolest.
Tabela 1
Dijabetes melitus tip 2
|
Etiologija |
Nasljedna predispozicija (podudarnost kod jednojajčanih blizanaca je i do 100%) na pozadini faktora okoline (gojaznost, urbani način života, višak rafiniranih masti i ugljikohidrata u ishrani) |
|
Patogeneza |
Inzulinska rezistencija, sekretorna disfunkcija β-ćelija (gubitak 1. brze faze lučenja insulina), hiperprodukcija glukoze u jetri |
|
Epidemiologija |
Oko 5-6% ukupne populacije, 10% odraslih, 20% ljudi starijih od 65 godina u zapadnim zemljama i Rusiji. Značajno veći u određenim etničkim grupama (50% među Indijancima Pima). Incidencija se udvostručuje svakih 15-20 godina |
|
Basic kliničke manifestacije |
Umjerena poliurija i polidipsija, komponente metaboličkog sindroma. Više od 50% slučajeva je asimptomatski. U trenutku postavljanja dijagnoze, većina ima kasne komplikacije različite težine |
|
Dijagnostika |
Skrining određivanje nivoa glikemije u rizičnim grupama i/ili u prisustvu simptoma dijabetesa |
|
DM-1, simptomatski (Cushingov sindrom, akromegalija, itd.) i rijetki oblici DM (MODY itd.) |
|
|
Hipokalorična dijeta, povećana fizička aktivnost, edukacija pacijenata, tabletirani hipoglikemijski lijekovi (metformin, sulfoniluree, tiazolidindioni, glinidi, inhibitori α-glikozidaze). Liječenje i prevencija kasnih komplikacija |
|
|
Invalidnost i mortalitet određuju se kasnim komplikacijama, obično makrovaskularnim |
Etiologija
T2DM je multifaktorska bolest s nasljednom predispozicijom. Konkordancija za T2DM kod identičnih blizanaca dostiže 80% ili više. Većina pacijenata sa T2DM ukazuje na prisustvo T2DM u njihovoj užoj porodici; Ako jedan od roditelja ima T2DM, vjerovatnoća njegovog razvoja kod potomka tokom života je 40%. Nije pronađen niti jedan gen, čiji polimorfizam određuje predispoziciju za T2DM. Faktori okoline, prvenstveno karakteristike životnog stila, igraju veliku ulogu u realizaciji nasljedne predispozicije za T2DM. Faktori rizika za razvoj T2DM su:
- gojaznost, posebno visceralna;
- etnička pripadnost (posebno kada se tradicionalni način života promijeni u zapadni);
- CD-2 kod bliskih rođaka;
- sjedilački način života;
- karakteristike ishrane (visoka potrošnja rafinisanih ugljenih hidrata i nizak sadržaj vlakna);
- arterijska hipertenzija.
Patogeneza
Patogenetski, T2DM je heterogena grupa metaboličkih poremećaja, što određuje njegovu značajnu kliničku heterogenost. Njegova patogeneza se zasniva na insulinskoj rezistenciji (smanjenju inzulinom posredovane iskorišćavanja glukoze u tkivima), koja se javlja u pozadini sekretorne disfunkcije β-ćelija. Dakle, postoji neravnoteža u insulinskoj osetljivosti i lučenju insulina. Sekretorna disfunkcija β-ćelija uključuje usporavanje „ranog” sekretornog oslobađanja insulina kao odgovor na povećane nivoe glukoze u krvi. U ovom slučaju, 1. (brza) faza sekrecije, koja se sastoji od pražnjenja vezikula akumuliranim inzulinom, praktički izostaje; 2. (spora) faza sekrecije javlja se kao odgovor na stabilizaciju hiperglikemije konstantno, u toničnom režimu, i, unatoč prekomjernoj sekreciji inzulina, nivo glikemije na pozadini inzulinske rezistencije se ne normalizira (slika 1).
Rice. 1. Sekretorna disfunkcija beta ćelija kod dijabetes melitusa tipa 2 (gubitak 1. brze faze lučenja insulina)
Posljedica hiperinzulinemije je smanjenje osjetljivosti i broja inzulinskih receptora, kao i supresija postreceptorskih mehanizama koji posreduju u djelovanju inzulina ( insulinska rezistencija). Sadržaj glavnog transportera glukoze u mišićnim i masnim ćelijama (GLUT-4) smanjen je za 40% kod osoba sa visceralnom gojaznošću i za 80% kod osoba sa T2DM. Zbog inzulinske rezistencije hepatocita dolazi do portalne hiperinzulinemije prekomjerna proizvodnja glukoze u jetri, a razvija se hiperglikemija natašte, koja se otkriva kod većine pacijenata sa T2DM, uključujući i rane faze bolesti.
Sama hiperglikemija negativno utiče na prirodu i nivo sekretorne aktivnosti β-ćelija (glukotoksičnost). Dugoročno, tokom mnogo godina i decenija, postojeća hiperglikemija na kraju dovodi do iscrpljivanja proizvodnje inzulina β-ćelija i pacijent može osjetiti neke simptome nedostatak insulina- mršavljenje, ketoza sa popratnim zarazne bolesti. Međutim, rezidualna proizvodnja inzulina, koja je dovoljna da spriječi ketoacidozu, gotovo je uvijek očuvana kod T2DM.
Dedov I.I., Melnichenko G.A., Fadeev V.F.
- kronična bolest koja je rezultat inzulinske rezistencije i relativnog nedostatka inzulina.
Etiologija dijabetes melitusa tipa 2
Multifaktorska bolest s nasljednom predispozicijom (ako jedan od roditelja ima dijabetes tipa 2, vjerovatnoća njegovog razvoja kod potomstva tokom života je 40%).
Faktori rizika za razvoj dijabetesa tipa 2 su:
- Gojaznost, posebno visceralna
- Etnička pripadnost
- Sjedilački način života
- Nutritional Features
- Arterijska hipertenzija
Patogeneza dijabetes melitusa tipa 2
Osnova je sekretorna disfunkcija beta stanica, koja se sastoji od usporavanja ranog sekretornog oslobađanja inzulina kao odgovora na povećanje razine glukoze u krvi.
U ovom slučaju, 1. (brza) faza sekrecije, koja se sastoji od pražnjenja vezikula akumuliranim inzulinom, praktički izostaje, a 2. (spora) faza sekrecije se javlja kao odgovor na stabilizaciju hiperglikemije konstantno, u toničnom režimu, i uprkos prekomjerno lučenje inzulina, razina glikemije se ne normalizira u pozadini inzulinske rezistencije.
Posljedica hiperinzulemije je smanjenje osjetljivosti i broja inzulinskih receptora, kao i supresija postreceptorskih mehanizama koji posreduju djelovanje inzulina (inzulinska rezistencija).
Sama hiperglikemija negativno utječe na prirodu i razinu sekretorne aktivnosti beta stanica - toksičnost glukoze. Dugotrajno, dugi niz godina i decenija, postojeća hiperglikemija u konačnici dovodi do iscrpljivanja proizvodnje inzulina beta stanicama i kod pacijenta se javljaju neki simptomi nedostatka inzulina - gubitak težine, ketoza uz prateće infektivne bolesti.
Kao rezultat, možemo razlikovati 3 nivoa:
- poremećeno lučenje insulina
- periferna tkiva postaju otporna
- povećava se proizvodnja glukoze u jetri
Dijagnostika dijabetes melitus tipa 2
- Mjerenje glukoze natašte (tri puta).
Normalan nivo glukoze u krvnoj plazmi natašte je do 6,1 mmol/l.
Ako je od 6,1 do 7,0 mmol/l – smanjena glukoza natašte.
Više od 7 mmol/l – dijabetes melitus. - Test tolerancije na glukozu. Provodi se samo ako su rezultati upitni, odnosno ako je glukoza od 6,1 do 7,0 mmol/l.
14 sati prije testa propisuje se gladovanje, zatim se vadi krv - utvrđuje se početni nivo glukoze, zatim se pacijentu daje da popije 75 grama glukoze rastvorene u 250 ml vode. Nakon 2 sata uzimaju krv i gledaju:
- ako je manji od 7,8, onda normalna tolerancija glukoze.
- ako je od 7,8-11,1 onda poremećena tolerancija glukoze.
- ako je više od 11,1 onda SD. - Određivanje C-peptida je neophodno za diferencijalnu dijagnozu. Ako je dijabetes tipa 1, tada bi nivo C-peptida trebao biti bliži 0 (od 0-2); ako je iznad 2, onda dijabetes tipa 2.
- Ispitivanje glikoziliranog hemoglobina (indikator metabolizma ugljikohidrata u posljednja 3 mjeseca). Norma je manja od 6,5% do 45 godina starosti. Nakon 45 godina do 65 - 7,0%. Nakon 65 godina – 7,5-8,0%.
- Određivanje glukoze u urinu.
- Aceton u urinu, Langeov test.
- UAC, OAM, BH, glikemijski profil.
Kliničke manifestacije dijabetes melitus tipa 2
Postepeni početak bolesti. Simptomi su blagi (bez sklonosti ka ketoacidozi). Česta kombinacija sa gojaznošću (80% pacijenata sa dijabetesom) i arterijska hipertenzija.
Bolesti često prethodi sindrom insulinske rezistencije (metabolički sindrom): gojaznost, hipertenzija, hiperlipidemija i dislipidemija (visoka koncentracija triglicerida i niska koncentracija HDL holesterola), a često i hiperurikemija.
- Sindrom hiperglikemije (polidipsija, poliurija, svrab kože, gubitak težine od 10-15 kg za 1-2 mjeseca Jaka opća i mišićna slabost, smanjena učinkovitost, pospanost. Na početku bolesti, kod nekih pacijenata može doći do povećanja apetita)
- Glukozurija sindrom (glukoza u urinu).
- Sindrom akutnih komplikacija
- Sindrom kasnih kroničnih komplikacija.
Tretman dijabetes melitus tipa 2
Liječenje dijabetesa tipa 2 sastoji se od 4 komponente: dijetetske terapije, fizičke aktivnosti, oralnih hipoglikemijskih lijekova i terapije inzulinom.
Ciljevi tretmana
■ Glavni cilj liječenja pacijenata sa dijabetesom tipa 1 je kontrola glikemije.
■ Održavanje nivoa glikozilovanog hemoglobina.
■ Normalizacija opšteg stanja: kontrola visine, telesne težine, pubertet, praćenje krvnog pritiska (do 130/80 mm Hg), nivoa lipida u krvi (LDL holesterol do 3 mmol/l, HDL holesterol više od 1,2 mmol/l , trigliceridi do 1,7 mmol/l), kontrola funkcije štitnjače.
Ne liječenje lijekovima
Glavni zadatak liječnika je uvjeriti pacijenta u potrebu promjene načina života. Gubitak težine nije uvijek jedini cilj. Povećanje fizičke aktivnosti i promjene u režimu i ishrani također imaju blagotvoran učinak, čak i ako nije bilo moguće postići gubitak težine.
Ishrana
■ Principi ishrane kod dijabetesa tipa 2: pridržavanje normokalorične (ako je gojazno - hipokalorične) ishrane sa ograničavanjem zasićenih masti, holesterola i smanjenjem unosa lako probavljivih ugljenih hidrata (ne više od 1/3 svih ugljenih hidrata).
■ Dijeta br. 9 – osnovna terapija za pacijente sa dijabetesom tipa 2. Glavni cilj je smanjenje tjelesne težine kod gojaznih pacijenata. Praćenje dijete često dovodi do normalizacije metaboličkih poremećaja.
■ Ako imate višak kilograma - niskokalorična dijeta (≤1800 kcal).
■ Ograničavanje lako svarljivih ugljenih hidrata (slatkiši, med, zašećerena pića).
■ Preporučeni sastav hrane prema kalorijama (%):
✧ složeni ugljeni hidrati (tjestenine, žitarice, krompir, povrće, voće) 50–60%;
✧ zasićene masti (mlijeko, sir, životinjska mast) manje od 10%;
✧ polinezasićene masti (margarin, biljno ulje) manje od 10%;
✧ proteini (riba, meso, živina, jaja, kefir, mlijeko) manje od 15%;
✧ alkohol - ne više od 20 g/dan (uključujući kalorije);
✧ umjerena potrošnja zaslađivača;
✧ u slučaju arterijske hipertenzije potrebno je ograničiti konzumaciju kuhinjske soli na 3 g/dan.
Fizička aktivnost
Pojačava hipoglikemijski učinak inzulina, pomaže u povećanju sadržaja antiaterogenog LDL-a i smanjenju tjelesne težine.
■ Individualni odabir uzimajući u obzir starost pacijenta, prisustvo komplikacija i prateće bolesti.
■ Trebalo bi se preporučiti hodanje umjesto vožnje i penjanje stepenicama umjesto korištenja lifta.
■ Jedan od glavnih uslova je redovnost fizičke aktivnosti (na primjer, hodanje 30 minuta dnevno, plivanje 1 sat 3 puta sedmično).
■ Treba imati na umu da intenzivna fizička aktivnost može uzrokovati akutna ili odložena hipoglikemijska stanja, pa režim vježbanja treba „razraditi“ uz samokontrolu glikemije; ako je potrebno, doze treba prilagoditi hipoglikemijskih sredstava prije utovara.
■ Ako je koncentracija glukoze u krvi veća od 13–15 mmol/l, fizička aktivnost se ne preporučuje.
Tretman lijekovima dijabetes melitus tipa 2
Hipoglikemijski agensi
■ Ako nema efekta od dijetalne terapije i fizičke aktivnosti, propisuju se hipoglikemijski lijekovi.
■ Kada je glukoza u krvi natašte više od 15 mmol/l, oralni hipoglikemijski lijekovi se odmah dodaju dijetnom tretmanu.
1. Lijekovi koji pomažu u smanjenju inzulinske rezistencije (senzibilizatori).
Ovo uključuje metformin i tiazolidindione.
Početna doza metformina je 500 mg noću ili uz večeru. Nakon toga, doza se povećava za 2-3 grama u 2-3 doze.
Mehanizam djelovanja metformina:
- supresija GNG u jetri (smanjenje proizvodnje glukoze u jetri), što dovodi do smanjenja nivoa glukoze natašte.
-smanjenje insulinske rezistencije (povećana upotreba glukoze u perifernim tkivima, prvenstveno mišićima).
- aktivacija anaerobne glikolize i smanjenje apsorpcije glukoze u tankom crijevu.
Metformin je lijek izbora za gojazne pacijente. Liječenje metforminom kod gojaznih dijabetičara smanjuje rizik od kardiovaskularnih komplikacija i stopu smrtnosti. Metformin ne stimuliše lučenje insulina β-ćelijama pankreasa; dolazi do smanjenja koncentracije glukoze u krvi zbog inhibicije glukoneogeneze u jetri. Primjena metformina ne dovodi do razvoja hipoglikemije i ima povoljan učinak kod gojaznosti (u odnosu na druge antidijabetičke lijekove). Monoterapija metforminom dovodi do smanjenja tjelesne težine za nekoliko kilograma; Kada se lijek kombinira s derivatima sulfonilureje ili inzulinom, metformin sprječava debljanje.
Među nuspojavama, dispeptički simptomi su relativno česti. Budući da metformin nema stimulativno djelovanje na proizvodnju inzulina, hipoglikemija se ne razvija tijekom monoterapije ovim lijekom, odnosno njegovo djelovanje se označava kao antihiperglikemično, a ne hipoglikemijsko.
Kontraindikacije – trudnoća, teško zatajenje srca, jetre, bubrega i drugih organa
Tiazolidindioni (pioglitazon, rosiglitazon) su agonisti receptora gama aktiviranog proliferatorom peroksizoma (PPAR-gama).Tiazolidindioni aktiviraju metabolizam glukoze i lipida u mišićnom i masnom tkivu, što dovodi do povećanja aktivnosti endogenog insulina, tj. eliminacija insulinske rezistencije. Dnevna doza pioglitazon - 15-30 mg/dan, rosinlitazon -4-8 mg (za 1-2 doze.) Kombinacija tiazolidindina sa metforminom je veoma efikasna. Kontraindikacija za upotrebu je povećan nivo jetrenih transaminaza. Osim hepatotoksičnosti, nuspojave uključuju zadržavanje tekućine i edem, koji se češće razvijaju kada se lijekovi kombiniraju s inzulinom.
2. Lekovi koji utiču na beta ćelije i pojačavaju lučenje insulina (sekretogeni).
To uključuje sulfoniluree i derivate aminokiselina, koji se prvenstveno koriste nakon jela. Glavna meta lijekova sulfonilureje su beta ćelije otočića pankreasa. Lijekovi sulfonilureje se vezuju za specifične receptore na membrani beta ćelija, što dovodi do zatvaranja ATP-ovisnih kalijumskih kanala i depolarizacije ćelijskih membrana, što zauzvrat potiče otvaranje kalcijumskih kanala. Unošenje kalcija dovodi do njihove degranulacije i oslobađanja inzulina u krv.
Sulfonilureje: hlorpromazid.
Derivati aminokiselina: Gliklazid, početni – 40, dnevno – 80-320, 2 puta dnevno; glibenklamid; Glipizid; Gliquidone
3. Lijekovi koji smanjuju apsorpciju glukoze u crijevima.
To uključuje akarbozu i guar gumu. Mehanizam djelovanja akarboze je reverzibilna blokada alfa-glikozidaza u tankom crijevu, zbog čega se usporavaju procesi fermentacije i apsorpcije ugljikohidrata, smanjuje se brzina resorpcije i ulazak glukoze u jetru. Početna doza akraboze je 50 mg 3 puta dnevno, zatim se može povećati na 100 mg 3 puta dnevno, lijek se uzima neposredno prije jela ili za vrijeme obroka. Main nuspojave– crijevna dispepsija, koja je povezana s ulaskom neapsorbiranih ugljikohidrata u debelo crijevo.
4.Biguanidi.
Mehanizam: iskorištavanje glukoze mišićno tkivo pojačavanjem anaerobne glikolize u prisustvu endogenog ili egzogenog inzulina. Ovo uključuje metformin.
Prvo prepisujem monoterapiju, najčešće metformin - ako je glikiran hemoglobin do 7,5%.
Prepisuje se metformin u dozi od 850 mg 2 puta dnevno, postepeno povećavajući do 1000.
Ako je glikiran od 7,5 do 8,0%, onda dvokomponentni režim (sekretogen + metformin).
Više od 8,0% koristi insulinsku terapiju.
Ostalo lijekovi i komplikacije
■ Acetilsalicilna kiselina. Koristi se za liječenje pacijenata sa dijabetesom tipa 2 i kao primarna i sekundarna prevencija makrovaskularnih komplikacija. Dnevna doza - 100-300 mg.
■ Antihipertenzivi. Ciljna vrijednost za kompenzaciju dijabetesa tipa 2 je održavanje krvnog tlaka ispod 130/85 mm Hg, što pomaže u smanjenju smrtnosti od kardiovaskularnih komplikacija. Ako nema efekta od terapije bez lijekova (održavanje normalne tjelesne težine, smanjenje unosa soli, stres od vježbanja) prepisuje lekove. Lijekovi izbora su ACE inhibitori, koji, osim dobrog prognostičkog učinka na krvni tlak, smanjuju rizik od razvoja i napredovanja nefropatije. Ako su netolerantni, prednost se daje blokatorima receptora angiotenzina-II, blokatorima kalcijumskih kanala (nedehidropiridinski niz) ili selektivnim β-blokatorima. U kombinaciji sa koronarnom bolešću, preporučljivo je kombinirati ACE inhibitore i adrenergičke blokatore.
■ Dislipidemija. Kod dijabetesa tipa 2, dislipidemija se često javlja nezavisno. Među svim pokazateljima lipidnog spektra, najvažniji je održavanje nivoa LDL holesterola ispod 2,6 mmol/l. Da bi se postigao ovaj pokazatelj, koristi se dijeta sa niskim sadržajem holesterola (manje od 200 mg holesterola dnevno) uz ograničenje zasićenih masti (manje od 1/3 svih masti u ishrani). Ako je dijetalna terapija neefikasna, statini su lijekovi izbora. Terapija statinima je preporučljiva ne samo kao sekundarna, već i kao primarna prevencija razvoja koronarne arterijske bolesti i makroangiopatija.
■ Trigliceridi. Kompenzacija metabolizma ugljikohidrata u mnogim slučajevima ne dovodi do normalizacije nivoa triglicerida. Za izoliranu hipertrigliceridemiju, lijekovi izbora su derivati fibrinske kiseline (fibrati). Ciljane vrijednosti triglicerida za dijabetes tipa 2 su ispod 1,7 mmol/l. Za kombinovanu dislipidemiju, statini su lekovi izbora.
■ Nefropatija. Nefropatija je česta komplikacija dijabetesa tipa 2; na početku bolesti do 25-30% pacijenata ima mikroalbuminuriju. Liječenje nefropatije počinje u fazi mikroalbuminurije, a lijekovi izbora su ACE inhibitori. Normalizacija krvnog tlaka u kombinaciji s primjenom ACE inhibitora dovodi do smanjenja progresije nefropatije. Kada se pojavi proteinurija, ciljni krvni pritisak se pooštravaju (do 120/75 mmHg).
■ Polineuropatija. Neuropatija je jedan od glavnih uzroka nastanka čireva na nogama (sindrom dijabetičkog stopala). Dijagnoza periferne neuropatije postavlja se na osnovu proučavanja vibracije i taktilne osjetljivosti. Triciklički antidepresivi i karbamazepin se koriste u liječenju bolnih oblika periferne neuropatije.
■ Autonomne neuropatije. Ciljevi liječenja su ublažavanje simptoma ortostatske hipotenzije, gastropareze, enteropatije, erektilne disfunkcije i neurogene bešike.
■ Retinopatija. Otprilike 1/3 pacijenata s novodijagnosticiranim dijabetesom tipa 2 ima retinopatiju. Ne postoji patogenetski tretman za dijabetičku retinopatiju; laserska fotokoagulacija se koristi za smanjenje progresije proliferativne dijabetičke retinopatije.
■ Katarakta. Dijabetes je povezan sa brzim razvojem katarakte; kompenzacija dijabetesa može usporiti proces zamućenja sočiva.
Dalje zbrinjavanje pacijenta
■ Samokontrola glikemije - na početku bolesti i tokom dekompenzacije svakodnevno.
■ Glikozilirani hemoglobin - jednom u 3 mjeseca.
■ Biohemijski test krvi (ukupni proteini, holesterol, trigliceridi, bilirubin, aminotransferaze, urea, kreatinin, kalijum, natrijum, kalcijum) - jednom godišnje.
■ Opća analiza krv i urin - jednom godišnje.
■ Određivanje mikroalbuminurije - 2 puta godišnje od trenutka dijagnoze dijabetesa.
■ Praćenje krvnog pritiska – pri svakoj poseti lekaru.
■ EKG - jednom godišnje.
■ Konsultacije sa kardiologom - jednom godišnje.
■ Pregled stopala – pri svakoj poseti lekaru.
■ Pregled kod oftalmologa (direktna oftalmoskopija sa širokom zenicom) - jednom godišnje od trenutka postavljanja dijagnoze DM, češće po indikacijama.
■ Konsultacije sa neurologom - jednom godišnje od trenutka dijagnoze dijabetesa.
Edukacija pacijenata
Neophodno je educirati pacijenta po programu „Škola za dijabetičare tipa 2“. Svaka kronična bolest zahtijeva od pacijenta da stekne razumijevanje od čega boluje, sa čime se suočava i šta treba učiniti da spriječi invalidnost iu hitnim slučajevima. Pacijent mora biti orijentiran u taktici liječenja i parametrima njegove kontrole. Mora biti sposoban da samostalno prati stanje (ako je tehnički moguće) i poznaje taktiku i redoslijed laboratorijskog i fizikalnog praćenja bolesti, te nastojati samostalno spriječiti razvoj komplikacija bolesti. Program za oboljele od dijabetesa uključuje nastavu o općim pitanjima dijabetesa, ishrani, samokontroli, liječenje lijekovima i prevenciju komplikacija. Program u Rusiji postoji već 10 godina, pokriva sve regione i doktori znaju za njega. Aktivna edukacija pacijenata dovodi do poboljšanja metabolizma ugljikohidrata, smanjenja tjelesne težine i metabolizma lipida.
Najčešći način samokontrole, bez upotrebe ikakvih instrumenata, je određivanje glukoze u krvi pomoću test traka. Kada se kap krvi nanese na test traku, dolazi do hemijske reakcije koja uzrokuje promjenu boje. Boja test trake se zatim upoređuje sa skalom boja koja je odštampana na bočici u kojoj su pohranjene test trake i na taj način se vizuelno određuje nivo glukoze u krvi. Međutim, ova metoda nije dovoljno precizna.
Više efektivna sredstva samokontrola je upotreba glukometara - pojedinačnih uređaja za samokontrolu. Kada se koriste glukometri, proces analize je potpuno automatiziran. Potrebno za analizu minimalni iznos krv. Osim toga, glukometri su često opremljeni memorijom koja vam omogućuje snimanje prethodnih rezultata, što je korisno za upravljanje dijabetesom. Glukometri su prenosivi, precizni i jednostavni za upotrebu. Danas postoji mnogo vrsta glukometara. Sve vrste uređaja imaju svoje karakteristike upotrebe, s kojima se morate upoznati koristeći upute. Trake za glukometar, kao i one vizualne, su za jednokratnu upotrebu, a za glukometar određene kompanije prikladne su samo trake koje proizvodi proizvođač. Idealno za samokontrolu - mjerenje šećera u krvi na prazan želudac prije glavnih obroka i 2 sata nakon jela, prije spavanja. Potrebno je često mjerenje glikemije pri odabiru doze za inzulinsku terapiju i dekompenzaciju. Kada je kompenzacija postignuta i nema loše osećanje moguća je rjeđa samokontrola.
Određivanje šećera u urinu je manje informativan način za procjenu stanja organizma, jer ovisi o individualnom „bubrežnom pragu“ i predstavlja prosječan nivo šećera u krvi od posljednjeg mokrenja, a ne odražava stvarne fluktuacije šećera u krvi.
Druga metoda samokontrole je određivanje sadržaja acetona u urinu. Po pravilu, aceton u urinu se mora odrediti ako nivo glukoze u krvi duže vrijeme prelazi 13,0 mmol/l ili je nivo glukoze u urinu 2% ili više, kao i ako dođe do naglog pogoršanja zdravlja, ako se pojave znaci pojave dijabetičke ketoacidoze (mučnina, povraćanje, miris acetona iz usta i sl.) i kada se jave druge bolesti. Otkrivanje acetona u urinu ukazuje na rizik od razvoja dijabetička koma. U tom slučaju, odmah se obratite ljekaru.
Prognoza
Održavanje normalnog nivoa glukoze može odgoditi ili spriječiti razvoj komplikacija.
Prognoza je određena razvojem vaskularnih komplikacija. Incidencija kardiovaskularnih komplikacija kod pacijenata sa dijabetesom (9,5-55%) značajno je veća nego u opštoj populaciji (1,6-4,1%). Rizik od razvoja koronarne arterijske bolesti kod dijabetičara s pratećom hipertenzijom povećava se 14 puta tokom 10 godina života. Kod pacijenata sa dijabetesom, učestalost lezija je naglo povećana donjih udova sa razvojem gangrene i naknadnom amputacijom.
Ključne riječi
INSULINSKA RESISTENCIJA / DIJABETES MELITUS TIPA 2 / UPOTREBA GLUKOZE TKIVA/M-INDEX/ OŠTEĆENA GLIKEMIJA NA GLAS / poremećena TOLERANCIJA GLUKOZE/ INZULINSKA RESISTENCIJA / DIJABETES MELITUS TIPA 2 / KORIŠĆENJE GLUKOZE U TKIVAMA/ M-INDEKS / poremećena glikemija na post / poremećena TOLERANCIJA GLUKOZEanotacija naučni članak o kliničkoj medicini, autor naučnog rada - Mayorov Alexander Yurievich
U članku je dat pregled mehanizama poremećene insulinske osjetljivosti u procesu evolucije poremećaja metabolizma ugljikohidrata: od poremećena glikemija natašte(NGN) do poremećena tolerancija glukoze(NTG) i dijabetes melitus tipa 2(SD2). Razmatraju se receptorski i postreceptorski poremećaji iskorištavanje glukoze u tkivima, Utjecaj na insulinska rezistencija(IR) faktori kao što su glukotoksičnost i lipotoksičnost. Iznosimo vlastite podatke o proučavanju IR kod pacijenata s različitim poremećajima metabolizma ugljikohidrata. Izraženije smanjenje inzulinske osjetljivosti zabilježeno je kod T2DM nego kod IGT i IGN (u prosjeku za 50, 25 i 15%, respektivno, u poređenju sa zdravim osobama). Pokazane su značajne korelacije M-indeksa sa indeksom tjelesne mase (BMI) i nivoom metaboličke kontrole (HbA1c, trigliceridi). Analizirane su razlike u kliničkim i biohemijskim parametrima kod pacijenata sa T2DM u zavisnosti od stepena IR. Proučavanjem niza hormona i citokina utvrđeno je da su nivoi adiponektina i rezistina kod pacijenata sa T2DM niži u odnosu na zdrave osobe, a nivoi faktora tumorske nekroze-alfa i proinzulina viši. Prikazani su podaci o poboljšanju inzulinske osjetljivosti tijekom liječenja metforminom, pioglitazonom i inzulinom, uključujući i pacijente s ranim poremećajima metabolizma ugljikohidrata. Rezultati studije ukazuju na potrebu intenziviranja terapije za snižavanje glukoze bez čekanja na izraženo pogoršanje inzulinske osjetljivosti.
Povezane teme naučni radovi o kliničkoj medicini, autor naučnog rada - Mayorov Alexander Yurievich
-
Mehanizmi poremećenog metabolizma glukoze kod osoba sa "predijabetesom"
2009. / Dreval A.V., Misnikova I.V., Trigolosova I.V., Barsukov I.A. -
Pokazatelji metabolizma ugljikohidrata i proizvodnje inkretina kod pacijenata s morbidnom gojaznošću, uključujući i one koji su bili podvrgnuti biliopankreasnoj bajpasu
2014 / Dedov I. I., Melnichenko G. A., Troshina E. A., Mazurina N. V., Ogneva N. A., Yashkov Yu. I., Ilyin A. V. -
Predijabetes i novodijagnosticiran dijabetes melitus tipa 2: metabolički aspekti i hemostaza
2017 / Ametov Aleksandar Sergejevič, Petrik Galina Georgijevna, Kosmačeva Elena Dmitrijevna, Kartavenkov Sergej Aleksandrovič, Bratchik Ana Viktorovna -
Veza između nivoa leptina i kliničko-metaboličkih parametara pacijenata sa različitim tipovima novodijagnostikovanog predijabetesa
2017 / Sukhanova Olga Sergejevna, Dvorjašina Irina Vladimirovna -
Razvoj poremećaja metabolizma ugljikohidrata iz perspektive kronobiologije
2018 / Yuzhakova A.E., Nelaeva A.A., Khasanova Yu.V. -
Čimbenici povezani s abnormalnim kardio-gležnjačkim vaskularnim indeksom kod pacijenata s dijabetesom melitusom tipa 2 i predijabetesom
2016 / Sumin Aleksej Nikolajevič, Bezdenježnih Natalija Aleksandrovna, Fedorova Natalija Vasiljevna, Ščeglova Ana Viktorovna, Indukaeva Elena Vladimirovna, Artamonova Galina Vladimirovna -
Regulacija lučenja glukagona hormonima inkretina kod osoba s faktorima rizika za dijabetes melitus tipa 2
2014 / Shestakova E.A., Ilyin A.V., Deev A.D., Shestakova M.V., Dedov I.I. -
Optimiziranje skrininga za rano otkrivanje poremećaja metabolizma ugljikohidrata
2014 / Misnikova I.V., Dreval A.V., Kovaleva Yu.A., Gubkina V.A., Lakeeva T.S. -
Učinak metformina na metabolizam ugljikohidrata i lipida kod osoba s ranim poremećajima metabolizma ugljikohidrata
2010 / Dreval Aleksandar Vasiljevič, Misnikova Inna Vladimirovna, Trigolosova Irina Vladimirovna, Tišenina Raisa Stepanovna -
Lučenje leptina kod žena sa prekomjernom težinom u zavisnosti od stepena poremećaja metabolizma ugljikohidrata
2013 / Dreval Aleksandar Vasiljevič, Trigolosova Inna Vladimirovna, Misnikova Irina Vladimirovna
Ovaj pregled se fokusira na mehanizme poremećene osjetljivosti na inzulin povezane s evolucijom poremećaja metabolizma ugljikohidrata od povećane glikemije natašte (EFG) do poremećene tolerancije na glukozu (IGT) i dijabetesa tipa 2. Razmatraju se poremećaji iskorištenja glukoze na receptorskom i postreceptorskom nivou zajedno sa ulogom glukoze i lipotoksičnosti. Prikazani su originalni podaci o inzulinskoj rezistenciji (IR) kod pacijenata sa poremećajem metabolizma ugljikohidrata. Pokazalo se da je osjetljivost na inzulin kod DM2, EFG i IGT 50, 25 i 15% niža nego kod normalnih subjekata. M-indeks pozitivno korelira sa BMI i kvalitetom metaboličke kontrole (nivoa HbA1c i triglicerida). Analizirane su razlike u kliničkim i biohemijskim karakteristikama pacijenata sa DM2 u zavisnosti od stepena IR. Pokazalo se da su nivoi adiponektina i rezistina u DM2 niži nego kod zdravih osoba, dok se nivoi TNF-a i proinzulina povećavaju. Terapija metforminom, pioglitazonom i inzulinom poboljšava osjetljivost na inzulin čak i kod pacijenata s ranim poremećajima metabolizma ugljikohidrata. Zaključuje se da intenzivnu hipoglikemijsku terapiju treba započeti prije nego što se razvije izraženo pogoršanje osjetljivosti na inzulin.
Tekst naučnog rada na temu “Inzulinska rezistencija u patogenezi dijabetes melitusa tipa 2”
Inzulinska rezistencija u patogenezi dijabetes melitusa tipa 2
Mayorov A.Yu.
Istraživački centar Federalnog državnog univerziteta endokrinologije, Moskva (direktor - akademik Ruske akademije nauka i Ruske akademije medicinskih nauka I.I. Dedov)
Članak daje pregled mehanizama poremećene insulinske osjetljivosti u evoluciji poremećaja metabolizma ugljikohidrata: od poremećene glukoze natašte (IFG) do poremećene tolerancije na glukozu (IGT) i dijabetes melitusa tipa 2 (T2DM). Razmatraju se receptorski i postreceptorski poremećaji iskorišćenja glukoze u tkivima, uticaj faktora kao što su toksičnost glukoze i lipotoksičnost na insulinsku rezistenciju (IR). Iznosimo vlastite podatke o proučavanju IR kod pacijenata s različitim poremećajima metabolizma ugljikohidrata. Izraženije smanjenje inzulinske osjetljivosti zabilježeno je kod T2DM nego kod IGT i IGN (u prosjeku za 50, 25 i 15%, respektivno, u poređenju sa zdravim osobama). Pokazane su značajne korelacije M-indeksa sa indeksom tjelesne mase (BMI), nivoom metaboličke kontrole (HbL]C, trigliceridi). Analizirane su razlike u kliničkim i biohemijskim parametrima kod pacijenata sa T2DM u zavisnosti od stepena IR. Proučavanjem niza hormona i citokina utvrđeno je da su nivoi adiponektina i rezistina kod pacijenata sa T2DM niži u odnosu na zdrave osobe, a nivoi faktora tumorske nekroze-alfa i proinzulina viši. Prikazani su podaci o poboljšanju inzulinske osjetljivosti tijekom liječenja metforminom, pioglitazonom i inzulinom, uključujući i pacijente s ranim poremećajima metabolizma ugljikohidrata. Rezultati studije ukazuju na potrebu intenziviranja terapije za snižavanje glukoze bez čekanja na izraženo pogoršanje inzulinske osjetljivosti.
Ključne riječi: inzulinska rezistencija, dijabetes melitus tip 2, iskorištenje glukoze u tkivu, M-indeks, poremećena glikemija natašte, poremećena tolerancija glukoze
Inzulinska rezistencija u patogenezi dijabetes melitusa tipa 2
Endokrinološki istraživački centar, Moskva
Ovaj pregled se fokusira na mehanizme poremećene osetljivosti na insulin povezan sa
evolucija poremećaja metabolizma ugljikohidrata od povećane glikemije natašte (EFG) do poremećene tolerancije na glukozu (IGT) i dijabetesa tipa 2. Razmatraju se poremećaji iskorištenja glukoze na receptorskom i postreceptorskom nivou zajedno sa ulogom glukoze i lipotoksičnosti. Prikazani su originalni podaci o inzulinskoj rezistenciji (IR) kod pacijenata sa poremećajem metabolizma ugljikohidrata. Pokazalo se da je osjetljivost na inzulin kod DM2, EFG i IGT 50, 25 i 15% niža nego kod normalnih subjekata. M-indeks pozitivno korelira sa BMI i kvalitetom metaboličke kontrole (nivoa HbAlc i triglicerida). Analizirane su razlike u kliničkim i biohemijskim karakteristikama pacijenata sa DM2 u zavisnosti od stepena IR. Pokazalo se da su nivoi adiponektina i rezistina u DM2 niži nego kod zdravih osoba, dok se nivoi TNF-a i proinzulina povećavaju. Terapija metforminom, pioglitazonom i inzulinom poboljšava osjetljivost na inzulin čak i kod pacijenata s ranim poremećajima metabolizma ugljikohidrata. Zaključuje se da intenzivnu hipoglikemijsku terapiju treba započeti prije nego što se razvije izraženo pogoršanje osjetljivosti na inzulin.
Ključne riječi: insulinska rezistencija, dijabetes melitus tipa 2, iskorištavanje glukoze u tkivima, M-indeks, poremećena glikemija natašte, poremećena tolerancija glukoze
Himsworth i Kerr prvi su upotrijebili izraz neosjetljivost na inzulin (sinonim za IR) da definiraju relativno slab odgovor na egzogeni inzulin kod gojaznih i dijabetičara. U širem smislu, IR se odnosi na smanjenje biološkog odgovora na jedan ili više efekata insulina. Međutim, češće se IR definira kao stanje koje je praćeno smanjenjem iskorištenja glukoze tkivima (GT) tijela pod utjecajem inzulina, tj. otpornost stanica različitih organa i tkiva na hipoglikemijski učinak inzulina. Ali budući da je biološki efekat insulina regulacija metaboličkih reakcija (metabolizam ugljenih hidrata, masti i proteina) i mitogenih procesa (procesi rasta, diferencijacija tkiva, sinteza DNK, transkripcija gena), savremeni koncept IR nije ograničen samo na parametre koji karakterišu samo metabolizam ugljikohidrata, ali uključuje i promjene u metabolizmu masti, proteina, funkciji endotelnih stanica, ekspresiji gena itd.
Uz pojam „inzulinska rezistencija“ postoji i pojam „sindroma inzulinske rezistencije“ (metabolički sindrom). To je kombinacija kliničkih i laboratorijskih manifestacija: poremećeni metabolizam ugljikohidrata: poremećena glukoza natašte (IFG), poremećena tolerancija glukoze (IGT) ili dijabetes, centralna gojaznost, dislipidemija (povećan nivo triglicerida i LDL,
smanjenje HDL-a), arterijska hipertenzija, povećanje nivoa trombotičkih i antifibrinolitičkih faktora i, u konačnici, visoka predispozicija za razvoj ateroskleroze i kardiovaskularne bolesti.
IR je centralni mehanizam u evoluciji dijabetesa tipa 2 (T2DM), kao i generaliziranog metaboličkog sindroma općenito. Usko je povezan sa kardiovaskularnim faktorima rizika, koji značajno doprinose nastanku koronarne bolesti srca, pa je za smanjenje rizika od komplikacija potrebno ne samo postići kompenzaciju metabolizma ugljikohidrata, već i sveobuhvatno korigovati druge metaboličke poremećaji.
Postoji mnogo radova posvećenih evoluciji IR u T2DM. Razvoj hiperglikemije kod T2DM povezan je i sa smanjenjem iskorištenja glukoze u perifernim tkivima i povećanjem proizvodnje glukoze u jetri, tj. otpornost jetre na djelovanje inzulina, koji potiskuje stvaranje glukoze u njoj.
Pokazan je uticaj na insulinsku osetljivost i genetske karakteristike. Dakle, srodnici u prvom stepenu sa poremećenom, pa čak i normalnom tolerancijom na glukozu imaju izraženu IR u poređenju sa pojedincima u kontrolnoj grupi. Uprkos velikom broju studija koje ukazuju na prisustvo genetske predispozicije za IR i T2DM, priroda ovih genetskih faktora ostaje uglavnom nejasna. To može biti
To je zbog činjenice da je razvoj bolesti kod različitih ljudi uzrokovan kombinacijom varijanti različitih gena, od kojih svaka sama po sebi ima mali učinak, što otežava identifikaciju ovih varijanti.
Metabolizam glukoze kod zdravih osoba i mehanizmi njegovog poremećaja
Normalno, nivoi glukoze se regulišu procesima koji ovise o insulinu i ne-ovisnim o insulinu, koji doprinose regulaciji glukoze natašte i posle obroka. Mozak i nervni sistem su uglavnom nezavisni od insulina; oni autonomno regulišu potrošnju glukoze kao izvora energije preko transportera glukoze 1 (GLUT-1). Mišićno i masno tkivo zavise od insulina. Mogu koristiti i glukozu i ketonska tijela. Vrsta izvora energije koji će koristiti prvenstveno je određena količinom inzulina povezanog sa ćelijskim insulinskim receptorima. U prisustvu velika količina Inzulinska ćelija prvenstveno koristi glukozu, aktivno je hvata i metabolizira ili stvara zalihe glukoze u obliku glikogena u mišićima ili kao masnoća u masnom tkivu, dok efikasno smanjuje nivo postprandijalne glikemije. Kada su razine inzulina niske, stanica prelazi na metabolizam ketona/slobodne masne kiseline sa smanjenom iskorištenošću glukoze, umjesto da koristi slobodne masne kiseline iz krvotoka kao izvor energije. Gastrointestinalni trakt(GIT) učestvuje u homeostazi glukoze, jer obezbeđuje snabdevanje organizma glukozom tokom varenja. Kod pacijenata sa IR ili IGT, dodatna apsorpcija glukoze iz gastrointestinalnog trakta pogoršava već narušene regulatorne mehanizme homeostaze glukoze. Osim toga, inkretini se oslobađaju u gastrointestinalnom traktu kao odgovor na unos hrane, hormoni koji pomažu u smanjenju postprandijalnog nivoa glikemije. Inzulin i glukagon koje luče otočići pankreasa regulišu homeostazu glukoze. Inzulin se luči kao odgovor na povećanje nivoa glukoze u plazmi. Izlučeni inzulin potiskuje proizvodnju glukoze u jetri (glikogenolizu i glukoneogenezu), stimulira iskorištavanje i skladištenje glukoze u jetri i reguliše korištenje glukoze u mišićima i, u manjoj mjeri, u masnom tkivu. Jetra obavlja dvije glavne funkcije koje zavise od razine inzulina. Kada su razine inzulina niske, kao što je stanje natašte, jetra proizvodi glukozu kroz glikogenolizu i glukoneogenezu i oslobađa je kako bi održala normalne razine glukoze natašte. Kada su razine inzulina umjerene ili značajno povišene, jetra prestaje proizvoditi glukozu i preuzima glukozu iz plazme, a zatim je skladišti kao glikogen.
U stanju apsolutnog posta (ovaj termin se koristi za označavanje posta) večina glukoza se metabolizira u tkivima neovisnim o inzulinu: 50% se apsorbira u mozgu, a 25% se koristi unutrašnje organe. Tkiva zavisna od insulina, prvenstveno mišići, odgovorni su za recikliranje preostalih 25% glukoze. Nakon što glukoza uđe u crijeva ili parenteralno, ova ravnoteža između UGT i proizvodnje glukoze u jetri je poremećena. U ovom slučaju, održavanje normalne homeostaze glukoze ovisi o tri vrlo precizno koordinirana procesa: lučenje inzulina, UGT i supresija proizvodnje glukoze u jetri.
Osjetljivost perifernih tkiva na inzulin određena je prisustvom specifičnih receptora, čija funkcija posreduje u stimulativnom djelovanju inzulina na UGT.
koji uključuju transportere glukoze (GLUT). Vezivanje insulina za receptor dovodi do širok rasponćelijske reakcije. Receptor obavlja tri glavne funkcije: 1) sa visokom specifičnošću, prepoznaje mjesta vezivanja za inzulin u molekulu i kombinuje sa ovim drugim pomoću α-podjedinice; 2) posreduje u prenosu odgovarajućeg signala u cilju aktiviranja intracelularnih procesa kroz konformacione promene i aktivaciju p-podjedinice tirozin kinaze; 3) vrši endocitozu (uranjanje u ćeliju) kompleksa hormonskih receptora, što dovodi do lizozomalne proteolize inzulina uz istovremeni povratak podjedinice na ćelijsku membranu.
Kod T2DM, poremećena aktivacija inzulinskog receptora se opaža u skeletnim mišićima. Poznato je da poremećaj autofosforilacije inzulinskog receptora može dovesti do prestanka dalje kaskade reakcija neophodnih za djelovanje inzulina i IR skeletnih mišića. Međutim, mehanizam smanjene aktivnosti inzulinskih receptora tirozin kinaze kod T2DM nije jasan. To je zbog sekundarnih metaboličkih promjena, a ne zbog mutacije gena za inzulinski receptor.
Aktivnost tirozin kinaze inzulinskog receptora dovodi do autofosforilacije inzulinskog receptora i do fosforilacije drugih ćelijskih supstrata. Takozvani proteini supstrata insulinskih receptora (IRS) igraju centralnu ulogu u posredovanju delovanja insulina. Supstrati inzulinskog receptora služe kao veza između insulinskog receptora i drugih intracelularnih supstrata, kao što je fosfoinozitid 3-kinaza (PI-3-kinaza). Kada je stimulirana insulinom, PI 3-kinaza pretvara fosfoinozitol (PI)-4 ili P1-4,5-fosfat u PI-3,4 ili P1-3,4,5-fosfat. PI-3,4,5-fosfat, uz pomoć PI-3-kinaze, osigurava mjesto adaptera za PH domenu serin/treonin specifične protein kinaze B (PKB) i fosfolipidno zavisne kinaze (PDK 1 i PDK 2 ). PKB je vjerovatno uključen u različite tkivne efekte inzulina, uključujući stimulaciju uzimanja glukoze, glikolizu, glikogena i sintezu proteina. Na primjer, PKB stimulira translokaciju GLUT-4 vezikula u citoplazmatsku membranu. Kod T2DM opisana je poremećena aktivacija PKV u skeletnim mišićima, uprkos normalan nivo ovaj protein. Druga studija je otkrila smanjenje nivoa fosforilacije aktivnosti IRS-1 i PI-3-kinaze u skeletnim mišićima kod T2DM kod mršavih i gojaznih pacijenata, kao i kod gojaznih pacijenata bez dijabetesa, što je moglo biti povezano sa 50- 60% sa smanjenom ekspresijom IRS-1 i p85 PI-3-kinaze.
Kada se formira sekundarni glasnik, aktivira se transport glukoze. To se događa uz pomoć transportera glukoze (GLUT) - proteina koji se nalaze na unutrašnjoj površini ćelijskih membrana i prenose glukozu u ćeliju. Do danas je poznato 11 članova porodice GLUT, ali samo njih 7 je pokazalo transportnu aktivnost, uz jasnu identifikaciju na nivou različitih organa i tkiva.
Kada se glukoza transportuje u ćeliju, pokreću se brojni intracelularni mehanizmi metabolizma glukoze. Glukoza se fosforilira glukokinazom i heksokinazom, a zatim se metabolizira na dva načina: sintezom glikogena i glikolizom. Ovi procesi se odvijaju uz sudjelovanje enzima pod kontrolom inzulina. Najvažnije su glikogen sintaza (kontrola stvaranja glikogena) i piruvat dehidrogenaza (regulacija oksidacije glukoze). U svim stanjima otpornim na inzulin, uključujući gojaznost i T2DM, smanjena sinteza glikogena je glavni intracelularni poremećaj odgovoran
za defekt u delovanju insulina. Štoviše, u slučaju pretilosti s normalnom ili poremećenom tolerancijom glukoze, može se djelomično nadoknaditi hiperglikemijom. Dalje napredovanje IGT-a sa gojaznošću do T2DM povezano je sa nemogućnošću hiperglikemije da nadoknadi ovaj defekt kod insulin-zavisnog UGT-a. Smanjenje aktivnosti piruvat dehidrogenaze također je pokazano u adipocitima i mišićima pacijenata sa T2DM, iako mnogi autori smatraju da je ovo smanjenje sekundarno zbog hipoinzulinemije i povećan nivo slobodnih masnih kiselina, drugi ne nalaze dokaze za to.
Može se pretpostaviti da pacijenti sa IGT i početkom T2DM imaju blagu IR zbog smanjenja broja inzulinskih receptora. Kod pacijenata sa visokom hiperglikemijom natašte i teškom IR preovlađuje postreceptorski defekt. Između dvije opisane manifestacije IR kod T2DM, relativna važnost receptorskih i postreceptorskih poremećaja varira: kako se IR intenzivira, težina postreceptorskog defekta se povećava.
Metabolički sindrom je najčešća manifestacija IR. Međutim, koncept IR stanja je mnogo širi. Klasični primjeri teške naslijeđene IR su leprekonizam, Rabson-Mendenhallov sindrom, IR tip A. Različiti faktori utiču na osjetljivost tkiva na inzulin: starost, spol, višak tjelesne težine i posebno distribucija masnog tkiva, arterijski pritisak prisustvo dislipidemije, ishemijska bolest bolesti srca, kao i niz somatskih bolesti, pušenje, porodična anamneza dijabetesa, kvalitet ishrane, nizak fizička aktivnost, zloupotreba alkohola, psihoemocionalni faktori, lijekovi. IR se javlja ne samo kod T2DM, već i kod drugih bolesti praćenih metaboličkim poremećajima. IR se javlja kod više od 25% praktično zdravih osoba bez gojaznosti, a njegova težina je uporediva sa težinom IR uočene kod pacijenata sa T2DM.
Proučavanjem prirodnog toka IR u različitim populacijama, ustanovljeno je da je riječ o kombinaciji dvije komponente: genetske, odnosno nasljedne i stečene. U porodicama pacijenata sa T2DM može se pratiti njegova nasljedna komponenta. Dakle, srodnici u prvom stepenu sa poremećenom, pa čak i normalnom tolerancijom na glukozu imaju izraženiju IR u odnosu na osobe u kontrolnoj grupi. Slični podaci dobijeni su iz studija na monozigotnim blizancima. Daljnji dokaz genetske predispozicije za T2DM je da kod nekih etničke grupe njegova prevalencija je izuzetno visoka. Na primjer, među stanovnicima ostrva Nauru (Mikronezija) iznosi 40%, a među Indijancima Pima (Arizona, SAD) prelazi 50%. Osim gena koji reguliraju metabolizam ugljikohidrata, geni uključeni u patogenezu gojaznosti također mogu utjecati na rizik od razvoja T2DM.
Oko 80-90% pacijenata sa T2DM ima prekomjerna težina tijelo ili gojaznost. Dakle, sa I. stadijumom gojaznosti, rizik od T2DM se povećava 2 puta, II stadijuma gojaznosti - 5 puta, III stepen- više od 10 puta. Raspodjela masti igra posebnu ulogu. Taloženje visceralne masti na abdomenu povezano je s poremećenom tolerancijom glukoze i IR, bez obzira na tjelesnu težinu. Masno tkivo se danas smatra jednim od endokrinih organa, koji su mjesto sinteze značajne količine hormona i biološki aktivnih peptida, od kojih većina utiče na povećanje IR. Postoje dokazi da mogu narušiti prijenos inzulinskog signala i uzrokovati IR u ranim fazama, u fazi pred-dijabetesa. U visceralnom tkivu pojačano je lučenje hormona koji pojačavaju IR (TOT-a, rezistin, visfatin, Sh-6 itd.).
a istovremeno je smanjeno izlučivanje hormona adiponektina koji smanjuje IR.
Sposobnost hiperglikemije da direktno naruši osjetljivost na inzulin i lučenje inzulina smatra se fenomenom "glukozetoksičnosti". Hronična hiperglikemija smanjuje inzulinom stimuliranu upotrebu glukoze smanjenjem translokacije GLUT-4 u mišićnim stanicama. Sposobnost slobodnih masnih kiselina da inhibiraju glikolizu također može doprinijeti razvoju IR, što se naziva lipotoksičnost. Slobodne masne kiseline smanjuju osjetljivost na inzulin smanjujući transport glukoze i fosforilaciju u mišićima.
materijali i metode
U svrhu proučavanja evolucije IR-a, pregledano je 320 pacijenata sa različitim poremećajima metabolizma ugljikohidrata, od čega 262 bolesnika sa T2DM, 36 sa IGN, 22 sa IGT, koji su pregledani i liječeni u Federalnoj državnoj ustanovi Endokrinološki istraživački centar. Kontrolnu grupu činilo je 38 zdravih osoba. Na početku, 136 pacijenata je bilo na dijetnoj terapiji, 147 pacijenata je primalo različite oralne hipoglikemijske lijekove (ODG), a 37 pacijenata je bilo na terapiji inzulinom. Među ispitanima bilo je 142 muškaraca i 216 žena, a starost pacijenata u prosjeku je 52,8±11,0 godina (21-77 godina). Trajanje bolesti u prosjeku je bilo 6,7±6,8 godina (0-25 godina), a kod 128 pacijenata prvi put su otkriveni poremećaji metabolizma ugljikohidrata. Prosječni BMI kod pacijenata bio je 29,8±4,9 kg/m2 (18,4-45,9 kg/m2). Normalna tjelesna težina (BMI<25 кг/м2) имели 16,4% больных, избыточный вес (ИМТ 25-30 кг/м2) - 39,4%, ожирение (ИМТ>30 kg/m2) - 44,2% pacijenata. Većina pacijenata je imala distribuciju trbušne masti.
Određivanje ukupnog holesterola, triglicerida, nivoa holesterola lipoproteina velika gustoća(HDL), holesterol lipoproteina niske gustine (LDL) rađeni su na biohemijskom analizatoru Spectrum kompanije Abbott (SAD) sa standardnim setovima kompanije, glikovanim hemoglobinom (HbAlc) i mikroalbuminurijom - na DCA2000+ analizatoru kompanije Bayer (Nemačka), glikemija - na Reflotron analizatoru iz Boehringer Mannheim (Njemačka).
Za određivanje sadržaja C-peptida i imunoreaktivnog inzulina (IRI) u krvnom serumu korišten je elektrohemiluminiscentni imunotest (ECLIA) korištenjem Elecsys C-peptida i Elecsys Insulin kompleta reagensa Roche Diagnostics (Švicarska). Metodom enzimske imunoeseje, korišćenjem komercijalnih kompleta, nivo proinzulina u krvnom serumu je određen na prazan želudac (Proinsulin ELISA, „Mercodia“). Nivo leptina (Leptin ELISA, DBC, Kanada), adiponektina (Human Adiponectin ELISA, BioVendor, Češka), rezistina (Human Resistin ELISA, BioVendor, Češka Republika) određivan je u krvnom serumu natašte primjenom enzimske imunosorbentne metode primjenom komercijalni setovi., grelin (Total Ghrelin ELISA, DSL ACTIVE, USA), visfatin (Human Visfatin ELISA, BioSource, USA), faktor nekroze tumora-alfa (Human TNF-a, Bender MedSystems, Austrija). Sadržaj C-reaktivnog proteina natašte u krvnom serumu određen je imunoturbidimetrijskom metodom korištenjem CRP (Latex) HS COBAS kompleta Roche Diagnostics (Švicarska).
Osetljivost perifernih tkiva na insulin određivana je metodom hiperinzulinemične euglikemijske kleme. Metoda se zasniva na kontinuiranom intravenozno davanje insulin i glukoza (slika 1). Brzina infuzije insulina bila je konstantna i iznosila je 1 mU/kg/min, tačnost brzine injekcije
Vrijeme, min
♦ Brzina infuzije glukoze, mg/kg/min
i Brzina infuzije insulina, med/kg/min
* Nivo glukoze u plazmi, mmol/l
Rice. 1. Metoda izvođenja hiperinsulinemične euglikemijske kleme
insulin je obezbeđivao Pilot A2 dozator špriceva kompanije Fresenius Vial (Francuska-Njemačka). Brzina davanja glukoze je promijenjena na način da se održi ciljni nivo glikemije (5,3 ± 0,3 mmol/l), a tačnost brzine primjene glukoze osiguran je volumetrijskim dozatorom INCA-ST Fresenius Vial (Francuska). -Nemačka). Ukupno trajanje studije je 4-6 sati.Brzinom davanja glukoze u stabilnom stanju određena je brzina UGT, koja je korištena za izračunavanje koeficijenta iskorištenosti (M-indeks), kao aritmetičkog prosjeka od 10-12 diskretnih vrijednosti brzine infuzije glukoze, podijeljene s tjelesnom težinom subjekta ili sa nemasnom tjelesnom masom, u 1 minuti.
Takođe, procena nivoa IR izvršena je korišćenjem strukturnog matematičkog modela zasnovanog na određivanju insulina i glukoze u plazmi natašte (FPG) – HOMA (homeostasis model assessment) – uz izračunavanje koeficijenata IR i sekrecije insulina.
IR indeks (HOMA-OT)=
Korelacija M-indeksa i HbA1c r = -0,398, str<0,0001 "
IRI (μU/ml) x FPG (mmol/l) 22.5
Funkcionalna aktivnost beta ćelija (HOMA-PB)=
20 x IRI (µU/ml)
FPG (mmol/l) - 3,5
Rezultati istraživanja i diskusija
Veza između inzulinske osjetljivosti i osnovnih kliničkih i biokemijskih parametara kod pacijenata s različitim poremećajima metabolizma ugljikohidrata
Prilikom proučavanja stepena oštećenja insulinske osetljivosti kod svih osoba sa poremećenim metabolizmom ugljenih hidrata, vrednost M-indeksa na inicijalnom pregledu je varirala od 0,15 do 12 mg/kg/min, u proseku 4,01+2,27 mg/kg/min, što je skoro 2 puta niže od pokazatelja zdravih osoba (7,72+1,89 mg/kg/min, p<0,001). Анализ распределения частот встречаемости показал, что у 20,4% пациентов М-индекс находился в пределах 2 мг/кг/мин, что можно расценивать как выраженное снижение чувствительности к инсулину. У 31,9% М-индекс был в интервале от 2 до 4 мг/кг/мин, что соответствует умеренному снижению, у 27,2% - в интервале от 4 до 6 мг/кг/мин - незначительное снижение, у 20,5% периферическая чувствительность соответствовала близким к нормальным показателям (выше 6 мг/кг/мин). Значения М-индекса были одинаковыми у мужчин (3,96+2,20 мг/кг/мин) и женщин (4,13+2,29 мг/кг/мин). Это противоречит некоторым литературным данным о влиянии пола на чувствительность
Rice. 2. Ovisnost osjetljivosti na inzulin od nivoa HbA]c kod pacijenata s poremećajem metabolizma ugljikohidrata
na inzulin kod zdravih osoba i u općoj populaciji pacijenata sa T2DM. Budući da literatura sadrži indicije o mogućnosti starosnih promjena osjetljivosti na inzulin, analizirali smo vrijednosti brzine UGT kod pacijenata s poremećajem metabolizma ugljikohidrata različitih dobnih skupina. Pokazalo se da je kod mladih pacijenata (ispod 30 godina starosti), posebno kod muškaraca, stopa UGT nešto viša, ali zbog malog broja ovih pacijenata razlika u M indeksu nije bila statistički značajna. Nivo M-indeksa nije zavisio od trajanja (r=0,13, p=0,087) i starosti nastanka bolesti (r=0,06, p>0,3).
Upoređivanjem nivoa IR i tjelesne težine pacijenata, utvrđena je značajna veza između BMI i M-indeksa u opštoj grupi (r = -0,31, p<0,0001). Большинство исследований подтверждают, что и общая жировая масса, и распределение по абдоминальному типу ассоциированы с ИР . Это подтверждается и улучшением чувствительности к инсулину в нашем исследовании при повторном ее исследовании у части больных с впервые выявленным СД после снижения массы тела: на фоне уменьшения ИМТ с 29,4+0,5 до 28,0+0,5 кг/м2 (р<0,01) скорость УГТ возросла с 2,11+0,42 до 4,73+1,13 мг/кг/мин (р<0,001). Также показана выраженная обратная зависимость М-индекса от окружности талии (ОТ) (г=-0,35, р=0,003) и меньшая - от окружности бедер (об) (г=-0,23, р=0,047) и их соотношения (ОТ/ОБ) (г=-0,23, р=0,049), что отражает влияние прежде всего степени висцерального ожирения на уровень чувствительности к инсулину.
Utvrđena je jaka inverzna korelacija između brzine UGT i stepena kompenzacije metabolizma ugljenih hidrata: nivo HbA1c (r = -0,40, p<0,0001) и уровня ГПН (г=-0,43, р<0,0001) (рис. 2). Пациенты, достигшие целевого уровня НЬА1с (менее 7%), имели достоверно более высокий М-индекс по сравнению
kod pacijenata sa teškom dekompenzacijom (HbA1c iznad 9%): 5,30+2,43 i 2,83+1,73 mg/kg/min, respektivno (p<0,001). Таким образом, можно сказать, что глюкозотоксич-ность играет существенную роль в развитии и усугублении ИР, что подтверждается данными литературы, в том числе о влиянии снижения гликемии на улучшение чувствительности к инсулину . В нашем исследовании степень снижения НЬА1с была взаимосвязана с чувствительностью к инсулину при повторном определении - наибольшее снижение НЬА1с, например, на фоне инсулинотерапии, сопровождалось наименьшей ИР (г=-0,59, р<0,01).
Pokazano je da postoji značajna inverzna korelacija između nivoa triglicerida i M-indeksa (r = -0,31, p<0,0001). Пациенты, достигшие целевого уровня триглицеридов (менее 1,7 ммоль/л), рекомендованного отечественными стандартами лечения СД , имели достоверно более высокий М-индекс по сравнению с больными, имеющими выраженную гиперлипидемию (уровень триглицеридов выше 2,2 ммоль/л): 4,30+2,45 и 2,85+1,62 мг/кг/мин, соответственно (р<0,001). Корреляция с уровнем холестерина была достоверной, но значительно слабее (г=-0,18, р=0,018). Не было отмечено достоверной корреляции с уровнями ЛПНП (г=-0,05, р=0,511) и ЛПВП (г=0,19, р=0,074).
U tabeli 1 prikazane su komparativne karakteristike bolesnika sa različitim poremećajima metabolizma ugljikohidrata i zdravih osoba. Postojala je ne samo značajna razlika u stopi UGT u svim grupama pacijenata u odnosu na kontrolnu grupu, već i razlika kod pacijenata sa T2DM u poređenju sa osobama sa IGT i IFN. Među pacijentima s poremećajem metabolizma ugljikohidrata, oni sa IGT su imali najmlađu životnu dob (41,5 + 11,4 godine) i, shodno tome, najraniji početak bolesti (40,1 + 11,4 godine). Nisu se međusobno razlikovali u BMI, OB, WC, nivoima ukupnog holesterola, HDL i LDL holesterola i triglicerida. Iako dijagnoza IGT uključuje i normalan nivo FPG i odgovarajući nivo IGN, kod ispitivanih osoba sa IGT nivo FPG je bio značajno niži u odnosu na one sa IGN (5,38 + 1,25 vs 6,54 + 0,41 mmol/l, p=0,018) . Postojala je ne samo značajna razlika u stopi UGT u svim grupama pacijenata u odnosu na kontrolnu grupu, već i razlika kod pacijenata sa T2DM u poređenju sa osobama sa IGT i IGN. Pacijenti sa T2DM imali su skoro 2 puta niži M-indeks u odnosu na zdrave osobe: 3,75+2,20 naspram 7,72+1,89 mg/kg/min (p<0,0001). Пациенты с ранними нарушениями углеводного обмена продемонстрировали М-индекс в 1,3-1,4 раза меньше по сравнению с группой контроля. При анализе частоты встречаемости показателей скорости УГТ у пациентов с различными нарушениями углеводного обмена выявлено следующее: в отличие от группы пациентов с СД2, в группах с НТГ и НГН не встречалось значений М-индекса ниже 2 мг/кг/мин. Нормальные показатели были только у 17% больных СД2 и у 46% и 43% больных с НТГ и НГН, соответственно. В группе с НТГ почти в 2 раза чаще отмечалось умеренное снижение чувствительности к инсулину (М-индекс от 2 до 4 мг/кг/мин), чем в группе НГН: 31 и 14%, соответственно.
Analizirajući vezu između periferne inzulinske osjetljivosti kod pacijenata sa T2DM, nije bilo značajne korelacije između stope UGT i dobi početka dijabetesa (r=0,07, p>0,3), OB (r=-0,19, p>0,1). ) , WC/TB (r=-0,24, p=0,055), nivo holesterola (r=-0,15, p=0,069). Kao i općenito, svi pacijenti s različitim poremećajima metabolizma ugljikohidrata pokazali su snažnu inverznu korelaciju M-indeksa sa BMI (r = -0,29, p<0,001), ОТ (г=-0,33, р=0,008), НЬА1с (г=-0,39, р<0,0001), ГПН (г=-0,34, р<0,0001), уровнем триглицеридов (г=-0,37, р<0,0001). Несколько парадоксальной выглядит умеренная прямая корреляция скорости УГТ с возрастом (г=0,22, р=0,005) и длительностью заболевания (г=0,24, р=0,002), что, скорее
Sve u svemu, to je povezano s upotrebom lijekova koji utječu na osjetljivost na inzulin kod nekih pacijenata. To potvrđuje i činjenica da ovakva korelacija nije pronađena kod pacijenata sa novodijagnostikovanim T2DM.
Radi proučavanja uloge smanjene insulinske osetljivosti u nastanku dijabetesa, analizirane su razlike u kliničkim i biohemijskim parametrima kod pacijenata sa dijabetesom tipa 2, koji su podeljeni u 5 grupa u zavisnosti od stepena IR. U 1. grupi su bili pacijenti sa izraženim smanjenjem insulinske osetljivosti (M koeficijent manji od 2 mg/kg/min), u 2. grupu - oni sa M u rasponu od 2 do 4 mg/kg/min (umereno smanjenje), 3. grupa 1. - pacijenti sa M od 4 do 6 mg/kg/min (manji pad), 4. - pacijenti sa M od 6 do 8 mg/kg/min (normalna osetljivost), 5. - pacijenti sa visokom osetljivošću (M-indeks iznad 8 mg/kg/min). Rezultati ove analize prikazani su u tabeli 2. Bolesnici sa nižim M-indeksom su bili okarakterisani višim BMI, WC i WC/WC, što još jednom odražava uticaj visceralne gojaznosti na razvoj IR. Glukotoksičnost negativno utiče na osetljivost perifernih tkiva na insulin: nivoi HbA1c i FPG su bili viši u grupi pacijenata sa T2DM sa niskim stopama UGT. Potvrđena je i lipotoksičnost koja se manifestuje u višim nivoima triglicerida kod pacijenata sa niskim vrednostima M-indeksa.
Nivoi hormona i citokina i njihov odnos s indikatorima osjetljivosti na inzulin
Proučavanjem niza hormona i citokina kod pacijenata sa različitim poremećajima metabolizma ugljikohidrata, ustanovljeno je da su nivoi adiponektina i rezistina kod pacijenata sa T2DM niži u odnosu na zdrave osobe, a nivoi faktora tumorske nekroze-alfa (TNF- a) i proinzulina bili su viši (Tabela 3). Kao što je poznato iz literature, nivo adiponektina je u pozitivnoj korelaciji sa insulinskom osetljivošću, a negativno sa masom visceralnog masnog tkiva. U našem istraživanju postojala je značajna direktna korelacija nivoa adiponektina sa M-indeksom (r=0,24, p=0,019) i slaba inverzna korelacija sa WC-om (r=-0,18, p=0,036) WC/TB (r= 0,21, p=0,041). Nije pronađena značajna korelacija sa BMI. Mehanizam utjecaja na osjetljivost perifernih tkiva na inzulin prvenstveno je u tome što adiponektin smanjuje opskrbu jetre NEFA i stimulira njihovu oksidaciju aktivacijom protein kinaze, pomažući u smanjenju proizvodnje glukoze u jetri. Nivoi leptina i visfatina nisu se značajno razlikovali. Poznato je da ekspresija leptina direktno zavisi od sadržaja lipida u ćelijama, najviše u potkožnom masnom tkivu. Iako je lučenje leptina masnim tkivom praćeno povećanjem IR, nismo pronašli značajnu korelaciju između nivoa leptina i M-indeksa. Slične razlike za adiponektin, rezistin i TOT-a uočene su i u fazi ranih poremećaja metabolizma ugljikohidrata. No, treba napomenuti da nije bilo značajnih razlika u razinama ovih hormona među pacijentima s različitim poremećajima metabolizma ugljikohidrata. Samo je nivo visfatina u grupi osoba sa IGT bio niži u odnosu na pacijente sa T2DM i IGN. Značajno viši nivo visoko specifičnog C-reaktivnog proteina (CRP) takođe je dokazan i kod pacijenata sa T2DM i kod osoba sa IFN i IGT u poređenju sa kontrolnom grupom.
Utjecaj različitih lijekova na osjetljivost na inzulin
Među lijekovima koji utiču na osjetljivost na inzulin, metform-min se smatra u prvoj fazi liječenja T2DM. U našem radu metformin je propisan za 16 pacijenata sa novodijagnostikovanim T2DM, IGT i IFN starosti 34-56 godina (prosjek starosti 47,5+9,0 godina) sa BMI od 22,6 do 45,9 kg/m2 (prosjek 31,6+6,7 kg/ m2). Svi pacijenti nisu primali šećer
Tabela 1
Uporedne karakteristike bolesnika s različitim poremećajima metabolizma ugljikohidrata i zdravih osoba
Indikatori dijabetesa tipa 2 (1) IGN (2) IGT (3) Kontrola (4) Razlika između grupa, p
Broj pacijenata, n 262 36 22 38
Spol, ženski/muški, % 58,4/41,6 66,7/33,3 59,1/40,9 68,4/31,6 NS
Starost, godine 54,1±10,3 51,4±11,9 41,5±11,4 39,5±13,8 p1-3<0,0001; р1-4<0,0001; р2-3=0,051; р2-4=0,010
Trajanje bolesti, godine 7,5±6,8 1,0±1,3 0,3±0,8 - p1-2=0,023; p1-3<0,0001; р2-3=0,007
Starost početka bolesti, godine 46,7±8,7 49,8±11,1 40,1±11,4 - p1-3=0,009; p2-3=0,051
Tjelesna težina, kg 83,0±15,1 91,3±19,1 83,8±18,3 70,7±16,6 r1-4<0,001; р2-4=0,002; р3-4=0,012
BMI, kg/m2 29,6±4,8 31,8±4,2 29,6±5,5 25,4±4,9 p1-4<0,001; р2-4<0,001; р3-4=0,007
WC, cm 100,7±11,4 102,4±17,3 93,0±8,2 72,8±9,9 p1-4<0,0001; р2-4=0,001; р3-4=0,021
OB, cm 109,1±10,9 110,1±8,2 105,0±11,1 98,1±6,8 p1-4=0,002; r2-4=0,008
WC/OB 0,92±0,07 0,93±0,11 0,89±0,02 0,74±0,07 p1-4<0,0001; р2-4=0,002; р3-4=0,013
HbA]c, % 8,7±2,0 5,7±0,7 5,9±0,9 5,1±0,5 p1-2<0,0001; р1-3<0,0001; р1-4<0,001
Holesterol, mmol/l 5,72±1,32 5,36±0,99 5,26±1,15 5,18±0,95 NS
HDL, mmol/l 1,31±0,41 1,57±0,47 1,25±0,52 1,70±0,45 p1-4=0,008; r3-4=0,042
LDL, mmol/l 3,59±1,18 3,39±0,99 3,44±0,88 3,40±0,59 NS
Trigliceridi, mmol/l 2,15±1,69 2,01±1,30 1,80±1,51 1,14±0,54 p1-4<0,001; р2-4=0,031
FPG, mmol/l 10,17±3,00 6,54±0,41 5,38±1,25 4,91±0,64 r1-2<0,0001; р1-3<0,0001; р1-4<0,0001; р2-3=0,018; р2-4<0,0001
M-indeks, mg/kg/min 3,75±2,20 5,95±2,24 5,71±1,93 7,72±1,89 p1-2=0,010; p1-3<0,001; р1-4<0,0001; р2-4=0,023; р3-4=0,010
tabela 2
Komparativne karakteristike pacijenata sa T2DM u zavisnosti od stepena IR
Indikatori M-indeks, mg/kg/min Razlika između grupa, str
Manje od 2 (1) 2-4 (2) 4-6 (3) 6-8 (4) Više od 8 (5)
Broj pacijenata, n 58 87 72 31 14
Spol, ženski/muški, % 63,2/36,8 60,7/39,3 56,5/43,5 42,1/57,2 50/50 Br.
Starost, godine 48,4±9,7 54,2±10,0 55,5±9,3 55,4±12,2 50,0±10,8 p1-2=0,012; p1-3<0,001; р1-4=0,012
Trajanje bolesti, godine 4,2±5,9 7,5±7,0 8,6±6,2 7,9±6,9 8,0±8,3 p1-2=0,016; p1-3<0,001; р1-4=0,021
Starost nastanka bolesti, godine 44,3±8,1 46,7±8,9 46,8±7,8 47,6±10,0 42,0±11,1 Br.
BMI, kg/m2 31,3±4,7 29,8±5,1 29,5±4,6 26,6±3,9 26,5±2,8 p1-4<0,001; р1-5=0,008; р2-4=0,006; р2-5=0,050; р3-4=0,017
WC, cm 105,3±11,0 100,7±10,8 97,8±10,1 93,8±9,4 96,7±6,4 p1-4=0,016
O cm 108,8±9,9 110,8±11,1 109,0±11,7 104,7±12,3 104,0±5,3 NS
WC/OB 0,97±0,07 0,91±0,07 0,90±0,07 0,90±0,08 0,93±0,04 p1-2=0,016; p1-3=0,008; r1-4=0,031
HbA]c, % 9,3±1,8 9,5±2,1 8,1±1,6 7,6±1,4 7,6±2,7 p1-3=0,002; p1-4<0,001; р1-5=0,019; р2-3=0,001; р2-4<0,001; р2-5=0,010; р3-5=0,049
FPG, mmol/l 11,39±3,43 11,19±3,01 9,60±1,98 8,56±2,12 8,34±3,50 p1-3=0,015; p1-4<0,001; р1-5=0,025; р2-3=0,004; р2-4<0,001; р2-5=0,020; р3-4=0,031; р3-5=0,050
Holesterol, mmol/l 5,97±1,51 5,67±1,33 5,52±1,28 5,60±1,50 4,91±0,90 NS
HDL, mmol/l 1,29±0,52 1,25±0,39 1,41±0,43 1,25±0,29 1,36±0,44 NS
LDL, mmol/l 3,49±1,41 3,61±1,22 3,53±1,06 3,82±1,34 3,08±1,00 NS
Trigliceridi, mmol/l 2,93±2,00 2,02±1,02 1,75±0,93 1,68±0,96 1,05±0,42 p1-2=0,033; p1-3<0,001; р1-4<0,003; р1-5<0,001; р2-5=0,005; р3-5=0,030
M-indeks, mg/kg/min 1,29±0,48 2,77±0,49 4,87±0,49 6,69±0,56 9,42±1,33 p za sve grupe<0,0001
snižavanje terapije, kontrola glikemije nije zadovoljila ciljne parametre. Studija je provedena prije i poslije
3 mjeseca nakon liječenja metforminom u dozi od 850-1700 mg. Prosječan nivo HbA1c smanjen je sa 7,6+2,1 na 6,2+0,9% (p<0,01); 50% больных достигли целевых значений НЬА1с (до 6,5%). Хорошо известно, что бигуаниды оказывают существенное влияние не только на нормализацию углеводного обмена, но также улучшают состояние липидного обмена . В изучаемой группе пациентов уровень холестерина снизился с 5,61+1,09 до 5,07+1,19 ммоль/л (р<0,05), 58% больных достигли нормы. Уровень триглицеридов снизился с 2,36+1,8 до 1,6+1,0
mmol/l (str<0,02), 83% достигли нормы. М-индекс, характеризующий степень ИР, у больных СД2 увеличился с 4,10+1,60 до 5,82+2,18 (р<0,01); в группе пациентов с НТГ и НГН - с 3,68+0,91 до 6,98+2,24 (р<0,001). Уровень СРБ снизился с 3,55+3,42 до 2,35+2,40 мг/л (р<0,01), висфатина - с 3,35+2,56 до 2,46+1,50 нг/мл (р<0,02). Достоверного изменения уровней адипонектина, лептина, резистина, грелина не отмечалось. Таким образом, полученные данные подтверждают возможность использования метформина до развития СД2, на стадиях нарушенной регуляции глюкозы, что было ранее показано в отношении профилактики СД2 .
Tabela 3
Nivo hormona i citokina u bolesnika s različitim poremećajima metabolizma ugljikohidrata i zdravih osoba
Indikatori DM 2 (1) IGN (2) IGT (3) Kontrolni (4) Razlika između grupa, p
Broj pacijenata, n 163 26 22 25
C-peptid, ng/ml 2,06±1,28 3,48±1,22 2,34±1,50 2,26±1,11 p1-2=0,002; p2-3=0,029; p2-4=0,009
IRI, μU/ml 15,6±10,3 16,2±10,4 15,4±8,4 8,9±8,6 p1-4<0,001; р2-4=0,012; р3-4=0,005
Proinzulin, pmol/ml 20,7±15,1 15,4±13,3 9,3±5,9 6,2±4,9 p1-4<0,0001; р2-4=0,016
Adiponektin, μg/ml 6,80±4,26 7,18±3,05 8,03±4,95 14,33±5,78 p1-4<0,0001; р2-4<0,001; р3-4=0,008
Resistin, ng/ml 3,41±1,56 3,49±1,12 3,21±1,28 4,54±1,94 p1-4=0,013; p2-4=0,024; r3-4=0,036
Grelin, pg/ml 53,0±38,4 19,0±12,7 10,7±9,1 48,3±42,1 p1-2=0,001; p1-3=0,005; p2-4=0,017; r3-4=0,035
Leptin, ng/ml 8,23±5,69 9,93±4,43 12,49±13,89 8,29±7,03 NS
Visfatin, ng/ml 3,07±1,88 3,17±1,93 1,24±1,40 2,25±1,86 p1-3=0,037; r2-3=0,045
T^-a, pg/ml 10,31±9,32 6,74±5,64 5,62±4,84 2,17±2,05 p1-4=0,004; p2-4=0,016; p3-4=0,051
CRP, mg/l 4,59±5,57 3,57±3,06 2,93±1,87 1,69±2,31 p1-4<0,001; р2-4=0,010; р3-4=0,033
M-indeks, mg/kg/min 3,56±2,07 6,12±2,34 5,66±1,84 7,43±1,68 p1-2=0,008; p1-3=0,004; p1-4<0,0001; р2-4=0,018; р3-4=0,010
Tiazolidindionski lijekovi su pronašli svoju primjenu u protekloj deceniji. Jedinjenja ove klase djeluju kao agonisti receptora gama (PPAR-Y) aktiviranog proliferatorom nuklearnog peroksizoma. Aktivacija PPAR-Y receptora modulira transkripciju brojnih gena povezanih s prijenosom inzulinskih efekata na stanice i uključenih u kontrolu glukoze i metabolizam lipida. Sproveli smo otvorenu, prospektivnu opservacionu studiju o efikasnosti i bezbednosti leka pioglitazon kod pacijenata sa T2DM. Studija je obuhvatila 81 pacijenta: 28 pacijenata u grupi koja je primala monoterapiju i 53 pacijenta u grupi kombinovane terapije. Grupa za monoterapiju uključivala je pacijente koji su prethodno bili na dijetnoj terapiji i nisu primali oralne hipoglikemijske lijekove (OHLD). Grupa kombinovane terapije uključivala je pacijente koji su primali jedan od PSSP (glibenklamid ili metformin), ali nisu imali zadovoljavajuću kontrolu glikemije. Pioglitazon je propisan svim pacijentima u dozi od 30 mg jednom dnevno, trajanje aktivne terapije u obje grupe je bilo 3 mjeseca. Nakon terapije pioglitazonom, uočena su poboljšanja u kontroli glikemije u svim liječenim grupama. U grupi koja je primala monoterapiju, nivo HbA1c je statistički značajno smanjen za 1,3±1,2% (sa 8,6±1,4 na 7,3±1,2%), nivo FPG za 1,6±2,2 mmol/l (sa 10,2±2,8 na 8,6±2,2 mmol/l ) i HOMA-IR indikator za 3,2±5,4 (sa 10,6±6,4 na 7,4±3, 8). Osim toga, došlo je do povećanja HOMA-PB za 9,7 ± 60,4 i smanjenja nivoa IRI za 4,1 ± 12,2 μU/ml, ali ove promjene nisu bile statistički značajne. U grupi na kombinovanoj terapiji, nivo HbA1c je statistički značajno smanjen za 0,8±0,8% (sa 8,4±1,2 na 7,6±1,1%), nivo FPG za 1,7±2,3 mmol/l (sa 9,9±2,7 na 8,2±2,0 mmol/l). l), HOMA-IR vrijednost za 3,7±5,7 (sa 9,3±5,9±6,4 do 5,6±2,9) i nivo IRI za 5,5±9,9 µU/ml (od 20,8±11,4 do 15,3±6,4 µU/ml). U ovoj grupi pacijenata došlo je do povećanja HOMA-FB za 3,0±44,6, ali isto tako nije bilo statistički značajno. Analiza podgrupa kombinovane terapije pokazala je da je u obe podgrupe došlo do statistički značajnog smanjenja nivoa HbA1c, FPG, HOMA-IR i IRI, ali nije bilo statističkih razlika između podgrupa za sve analizirane parametre na kraju terapije.
Kako bi se procijenio učinak inzulinske terapije na osjetljivost na inzulin, 43 pacijenta sa T2DM su pregledana prije i nakon primjene inzulina. Starost bolesnika bila je u prosjeku 56,1±8,6 godina (38-75 godina), trajanje bolesti u prosjeku 11,7±6,8 godina (4-31 godina). Prosječan BMI kod pacijenata bio je 29,5±5,3 kg/m2 (20,2-42,1 kg/m2). Za poređenje
Uticaj mono- i kombinovane insulinske terapije, pacijenti su randomizirani u 3 grupe: monoterapija insulinom u pojačanom režimu (n=20), kombinacija sa metforminom u dozi od 1500 mg/dan (n=11) i pioglitazonom 30 mg/ dan (n= 12). Ponovljeni pregled je obavljen 6 mjeseci nakon prelaska na inzulinsku terapiju. Vrijednost M-indeksa na inicijalnom pregledu u prosjeku je iznosila 2,4±1,6 mg/kg/min, što je 3 puta niže od vrijednosti zdravih osoba.
Nakon 6 mjeseci terapije inzulinom, kada je ponovo određena stopa UGT, zabilježeno je značajno povećanje od 2 puta - do 4,5±2,3 mg/kg/min (p<0,001). Значительно изменилось распределение частоты встречаемости отдельных значений (рис. 3). На фоне инсулинотерапии не выявлено показателей ниже 1 мг/кг/мин, в 2 раза (до 36%) уменьшилось количество пациентов, имеющих выраженное снижение М-индекса (от 1 до 3 мг/кг/мин), 48% имели чувствительность к инсулину от 3 до 7 мг/кг/мин ^ 25% исходно), в 5 раз (до 16%) увеличилась доля лиц с нормальной скоростью УГТ.
Povećanje tjelesne težine tokom terapije inzulinom u prosjeku je iznosilo 2,7 kg, BMI se povećao na 30,3±4,2 kg/m2 (p<0,05), соотношение ОТ/ОБ в целом по группе не изменилось - 0,9±0,1. Степень увеличения массы тела зависела от уровня ИР и была максимальной при исходном М-индексе менее 1 и более
4 mg/kg/min, u poređenju sa grupama 1-2 i 2-4 mg/kg/min. Stepen promjene brzine UGT određen je početnim nivoom periferne insulinske osjetljivosti (r = -0,55, p<0,01). В группе с исходным М-индексом менее 1 мг/кг/мин наблюдалось наибольшее увеличение среднего показателя (с 0,4±0,3 до 2,8±2,0, р<0,05), в то время как у пациентов с М-индексом более 4 мг/кг/мин достоверного изменения не отмечено (с 6,1±1,7 до 4,6±1,6, р>0,05), uprkos podjednako izraženom povećanju telesne težine u obe grupe. Pokazana je inverzna veza između stepena povećanja telesne težine i početnog BMI (r=-0,39, p<0,05). Наибольшие значения М-индекса на фоне инсулинотерапии наблюдались у больных с исходно нормальной массой тела: 7,2±2,3 vs 3,5±1,6; 4,1±1,9 мг/кг/мин, р<0,01. В процессе лечения средний уровень ГПН снизился с 13,3±3,1 до 9,6±2,4 ммоль/л (р<0,01), средний уровень НЬА1с - с 11,2±1,6 до 7,7±1,4% (р<0,01). Наибольшее снижение НЬА1с сопровождалось наименьшей ИР на фоне инсулинотерапии (г=-0,59, р<0,01), что отражает непосредственное влияние гипергликемии (глюкозотоксичность) на чувствительность к инсулину. Назначение инсулина приводило к значительному улучшению липидного профиля: снижению общего холестерина (5,4±1,1 ммоль/л, р<0,001), ЛПНП (3,4±1,0 ммоль/л, р=0,001) и триглицеридов (1,62±0,7 ммоль/л, р<0,001) Уровень ЛПВП холестерина достоверно не изменился.
0% od 0 do 1 na početku
od 1 do 2 od 2 do 3
tokom tretmana
Rice. 3. Distribucija pacijenata u zavisnosti od stepena IR na početku i tokom insulinske terapije 4.5
2,4±1,6 4,5±2,3
mg/kg/min
metformin
pioglitazon
tokom tretmana
* - R<0,05 по сравнения с исходными данными Рис.4. Динамика чувствительности к инсулину на фоне инсулинотерапии в разных лечебных группах
Korelacija je uočena samo sa nivoima triglicerida (r=-0,53, str<0,01). Показательно то, что изменения зафиксированы, несмотря на увеличение массы тела обследуемых за время инсулинотерапии. В группе больных с наименьшей степенью ИР показатели липидного профиля достигли значений, соответствующих низкому риску развития сосудистых осложнений.
U sve 3 grupe (monoinzulinska terapija, kombinacija sa metforminom 1500 mg/dan i pioglitazonom 30 mg/dan), insulinska terapija je sprovedena u intenziviranom režimu, što je posledica stepena pogoršanja metaboličke kontrole. Prilikom poređenja grupa prije početka terapije inzulinom nije bilo razlika u BMI, nivoima C-peptida, kao ni u nivou lipida, glikiranog hemoglobina i osjetljivosti na inzulin. Na pozadini terapije inzulinom zabilježena je pozitivna dinamika metaboličkih parametara u svim grupama.
troll, nisu uočene značajne razlike između grupa. Do poboljšanja insulinske osetljivosti tokom insulinske terapije došlo je u svim grupama podjednako: u grupi 1 - 1,8 puta, u grupi 2 - 2 puta i u grupi 3 - 2,2 puta, p>0,1 između grupa (slika 4). Prosječne dnevne doze inzulina kod pacijenata različitih grupa nisu se značajno razlikovale (0,66±0,2 vs 0,59±0,1 vs 0,57±0,6 U/kg/dan).
Tako je kod pacijenata sa novodijagnostikovanim T2DM, IGT i IGN pokazano prisustvo IR, što se manifestuje smanjenjem stope iskorišćenja glukoze u tkivima, merene metodom kleme. Istovremeno, došlo je do izraženijeg smanjenja inzulinske osjetljivosti kod T2DM nego kod IGT i IGN (u prosjeku za 50, 25 i 15%, respektivno, u poređenju sa zdravim osobama). Promjene u nivou IR tokom evolucije T2DM su sekundarne prirode, povezane sa toksičnošću glukoze, lipotoksičnošću, povećanjem tjelesne težine i terapijom za snižavanje glukoze. Sve to diktira potrebu za intenziviranjem terapije za snižavanje glukoze, uključujući prelazak na inzulinsku terapiju, bez čekanja na izraženo pogoršanje osjetljivosti na inzulin. Prilikom proučavanja uticaja hormona i citokina na IR parametre, otkrivena je značajna razlika u nivoima adiponektina, rezistina, proinzulina i TNF-a između zdravih osoba i pacijenata sa različitim poremećajima metabolizma ugljikohidrata. Propisivanje insulinske terapije dovodi do dvostrukog povećanja insulinske osetljivosti kod ispitivane kategorije pacijenata, direktno u zavisnosti od stepena poboljšanja glikemijske kontrole i uz istovremeno smanjenje aterogenosti lipidnog profila.
Zahvalnost na pomoći u obavljanju posla osoblju laboratorije kliničke biohemije (na čelu sa A.V. Ilyin) i laboratoriji za hormonsku analizu (predvodi profesor N.P. Goncharov) Federalne državne ustanove Endokrinološki istraživački centar.
Književnost
1. Himsworth H.P., Kerr R.B. Insulin-sensitive and Insulin-insensitive tips diabetes mellitus // Clin. Sci. - 1939. - br. 4. - R. 119-152.
2. Dedov I.I., Šestakova M.V. Dijabetes. - M.: Universum Publishing. - 2003.
3. Del Prato S., Leonetti F., Matsuda M., DeFronzo R.A. et al. Utjecaj trajne fiziološke hiperinzulinemije i hiperglikemije na lučenje inzulina i osjetljivost na inzulin kod čovjeka // Diabetologia. - 1994. - br. 37. - R. 1025-1035.
4. Balabolkin M.I., Klebanova E.M. Inzulinska rezistencija u patogenezi dijabetes melitusa tipa 2 // Diabetes mellitus. - 2001. -
br. 1. - str. 28-37.
5. Šestakova M.V., Breskina O.Yu. Inzulinska rezistencija: patofiziologija, kliničke manifestacije, pristupi liječenju // Consilium medicum. - 2002. - br. 10.
6. Kumar S., O"Rahily S. Inzulinska rezistencija. Djelovanje inzulina i njegovi poremećaji u bolestima // John Wiley & Sons, Ltd. - 2005.
7. Nathan D.M., Davidson M.B., DeFronzo R.A. et al. Poremećaj glukoze natašte i poremećena tolerancija glukoze // Diabetes Care. - 2007. - br. 30. - P. 753-759.
8. Reaven G.M. Uloga insulinske rezistencije u bolesti ljudi (sindrom X): proširena definicija // Annual Review of Medicine. - 1993. -
br. 44. - Str. 121 - 131.
9. Ba^a6o^KUH M.M. flua6eTo^orun. - M.: Megu^Ha. - 2000.
10. DeFronzo R.A. Lilly predavanje 1987. Trijumvirat: beta-ćelije, mišići, jetra. Dogovor odgovoran za NIDDM // Dijabetes. - 1988. - br. 37. - P. 667-687.
11. Abel E.D., Peroni O., Kim J.K., Kim Y.B., Boss O., Hadro E.,
Minnemann T., Shulman G. I., Kahn B. B. Adipozno-selektivno ciljanje gena GLUT4 narušava djelovanje inzulina u mišićima i jetri // Nature. -
2001. - br. 409. - str. 729-733.
12. Roden M., Price T.B., Perseghin G., Petersen K.F., Rothman D.L.,
Cline G.W., Shulman G.I. Mehanizam nastanka slobodnih masnih kiselina
insulinska rezistencija kod ljudi // J. Clin. Invest. - 1996. - Br. 97. -
13. Elrick H., Stimmler L., Hlad C.J., Turner D.A. Inzulinski odgovori plazme na oralnu i intravensku primjenu glukoze // J. Clin. Endocrinol Metab. - 1964. - br. 24. - R. 1076-1082.
14. Clark M.G., Wallis M.G., Barrett E.J., Vincent M.A., Richards S.M.,
Clerk L.H., Rattigan S. Protok krvi i mišićni metabolizam: fokus na djelovanje inzulina // Am. J. Physiol. - 2003. - br. 284. - R. E241-258.
15. Dedov I.I., Balabolkin M.I. Inzulinska rezistencija u patogenezi dijabetes melitusa tipa 2 i mogućnost lijeka za njeno prevladavanje // Doktor. - 2006. - br. 11.
16. Olefsky J.M. Inzulinski receptor Multifunkcionalni protein // Dijabetes. - 1990. - br. 39. - R. 1009-1016.
17. Bijeli M.F. IRS proteini i uobičajeni put do dijabetesa // Am J Physiol Endocrinol Metab. - 2002. - br. 283. - R. E413-422.
18. Kimber W.A., Deak M., Prescott A.R., Alessi D.R. Interakcija proteina tirozin fosfataze PTPL1 sa PtdIns(3,4)P2-vezujućim adapterskim proteinom TAPP1 // Biochem. J. - 2003. - Br. 376. - R. 525-535.
19. Heller-Harrison R.A., Morin M., Guilherme A., Češka M.P. Inzulinom posredovano ciljanje fosfatidilinozitol 3-kinaze na vezikule koje sadrže GLUT4 // J. Biol. Chem. - 1996. - br. 271. - R. 10200-10204.
20. Whiteman E.L., Cho H., Birnbaum M.J. Uloga Akt/protein kinaze B u metabolizmu // Trends Endocrinol Metab. - 2002. - br. 13. - R. 444-451.
21. Ueki K., Fruman D.A., Yballe C.M., Fassaur M., Klein J., Asano T.,
Cantley L.C., Kahn C.R. Pozitivne i negativne uloge p85alfa i p85beta regulatornih podjedinica fosfoinozitid 3-kinaze u inzulinskoj signalizaciji // J. Biol. Chem. - 2003. - br. 278. - R. 48453-48466.
22. Joost H. G., Bell G. I., Best J. D., Birnbaum M. J., Charron M. J., Chen Y. T., Doege H., James D. E., Lodish H. F., Moley K. H. et al. Nomenklatura GLUT/SLC2A familije olakšavatelja transporta šećera/poliola // Am. J. Physiol. - 2002. - br. 282. - R. E974-976.
23. Barzilai N., Rossetti L. Uloga glukokinaze i glukoza-6-fosfataze u akutnoj i kroničnoj regulaciji jetrenih tokova glukoze inzulinom // Biol. Chem. - 1993. - br. 268. - R. 25019-25025.
24. Printz R.L., Koch S., Potter L.R., O'Doherty R.M., Tiesinga J.J., Moritz S., Granner D.K. Heksokinaza II inzulinska mRNA i struktura gena, regulacija i evolucija // J. Biol. Chem. - 1993. - Ne. 268. -
25. Cohen P., Frame S. Renesansa GSK3 // Nat. Rev. Mol. Cell.
Biol. - 2001. - br. 2. - R. 769-776.
26. Harris R.A., Bowker-Kinley M.M., Huang B., Wu P. Regulacija aktivnosti kompleksa piruvat dehidrogenaze // Adv. Enzim Regul. - 2002. - br. 42. - R. 249-259.
27. Kahn S.E. Relativni doprinos insulinske rezistencije i disfunkcije beta-stanica patofiziologiji dijabetesa tipa 2 // Diabetologia. - 2005. - br. 48. - R. 3-19.
28. Reaven G.M. Uloga inzulinske rezistencije u bolesti ljudi // Dijabetes. - 1988. - br. 37. - R. 1595-1607.
29. Cassell P.G., Jackson A.E., North B.V., Evans J.C., Syndercombe-Court D., Phillips C., Ramachandran A., Snehalatha C., Gelding S.V., Vijayaravaghan S., Curtis D., Hitman G.A. Kombinacije haplotipova polimorfizama gena kalpain 10 povezuju se s povećanim rizikom od poremećene tolerancije glukoze i dijabetesa tipa 2 u Južno Indijanaca // Dijabetes. -
2002. - br. 51. - R. 1622-1628.
30. Haffner S.M., Karhapaa P., Mykkanen L., Laakso M. Inzulinska rezistencija, raspodjela tjelesne masti i polni hormoni kod muškaraca // Dijabetes. - 1994. - br. 43. - R. 212-219.
31. Peiris A.N., Struve M.F., Mueller R.A., Lee M.B., Kissebah A.H. et al. Metabolizam glukoze u gojaznosti: utjecaj distribucije tjelesne masti // J. Clin. Endocrinol. Metab. - 1988. - br. 67 (4). - R. 760-767.
32. Jazet I. M., Pijl H., Meinders A. E. Masno tkivo kao endokrini organ: utjecaj na inzulinsku rezistenciju // Neth. J. Med. - 2003. - br. 61 (6). -
33. Fasshauer M., Paschke1 R. Regulacija adipocitokina i inzulinska rezistencija // Diabetologia. - 2003. - br. 46. - R. 1594-1603.
34. Yki-Jarvinen H. Toksičnost glukoze // Endocr. Rev. - 1992. - br. 11. -
35. McGarry J.D., Dobbins R.L. Masne kiseline, lipotoksičnost i inzulinska rezistencija // Diabetologia. - 1999. - br. 42. - R. 128-138.
36. DeFronzo R.A., Tobin J.D., Andres R. Glucose clamp tehnika: metoda za kvantificiranje lučenja inzulina i rezistencije // American Journal of Physiology. - 1979. - br. 237 (3). - R. E214-223.
37. Matthews D.R., Hosker J.P., Rudenski A.S., Turner R.C. et al. Procjena modela homeostaze: inzulinska rezistencija i funkcija p-stanica iz glukoze u plazmi natašte i koncentracije inzulina u čovjeka // Diabetologia. - 1985. - br. 28. - R. 412-419.
38. Wallace T.M., Levy J.C., Matthews D.R. Upotreba i zloupotreba HOMA modeliranja // Diabetes Care. - 2004. - br. 27. - R. 1487-1495.
39. Nuutila P., Knuuti M.J., Maki M., Yki-Jarvinen H. et al. Spol i osjetljivost na inzulin u srcu i skeletnim mišićima. Studije pomoću pozitronske emisione tomografije // Dijabetes. - 1996. - br. 44 (1). - R. 31-36.
40. DeFronzo R. A., Bonadonna R. S., Ferrannini E. Patogeneza NIDDM.
Uravnotežen pregled // Diabetes Care. - 1992. - br. 15. - R. 318-368.
41. Frayn K.N. Visceralna masnoća i inzulinska rezistencija - uzročni ili korelativni? // Br J Nutr. - 2000. - br. 83 (Suppl. 1). - S71-77.
42. Rossetti L. Toksičnost glukoze: implikacije hiperglikemije u patofiziologiji dijabetes melitusa // Clin. Invest. Med. - 1995. -
br. 18. - R. 255-260.
43. Algoritmi za specijalizovanu medicinsku negu pacijenata sa dijabetes melitusom (priredili Dedov I.I., Shestakova M.V.). Četvrto izdanje, prošireno. - M., 2009. - 103 str.
44. Pittas A.G., Joseph N.A. Adipocitokini i inzulinska rezistencija // J. Clin. Endocrinol. Metab. - 2004. - br. 89. - R. 447-452.
45. Grupa UK Prospective Diabetes Study (UKPDS). Utjecaj intenzivne kontrole glukoze u krvi metforminom na komplikacije u bolesnika s prekomjernom tjelesnom težinom s dijabetesom tipa 2 (UKPDS 34) // Lancet. - 1998. - Br. 352. -
46. Prospektivna studija o dijabetesu u Ujedinjenom Kraljevstvu 24: 6-godišnje, randomizirano, kontrolirano ispitivanje koje upoređuje terapiju sulfonilureom, inzulinom i metforminom
kod pacijenata s novodijagnosticiranim dijabetesom tipa 2 koji se nije mogao kontrolirati dijetoterapijom // Ann. Intern. Med. - 1998. - br. 128 (3). - R. 165-175.
47. Knowler W.C., Barrett-Connor E., Fowler S.E. et al. Smanjenje incidencije dijabetesa tipa 2 uz intervenciju načina života ili metformin // N. Engl. J. Med. - 2002. - br. 346. - R. 393-403.
48. Semple R.K., Chatterjee V.K., O"Rahilly S. PPAR gama i ljudska metabolička bolest // J. Clin. Invest. - 2006. - Br. 116. - R. 581-589.
Mayorov Alexander Yurievich Doktor medicinskih nauka, šef. odjel za programsku obuku i liječenje, Federalna državna ustanova Endokrinološki istraživački centar,
Dijabetes spada u kategoriju endokrinih bolesti koje nastaju zbog relativnog ili apsolutnog nedostatka hormona inzulina. Hiperglikemija (trajno povećanje glukoze u krvi) može se razviti kao rezultat poremećaja u vezi inzulina sa tjelesnim stanicama.
Bolest karakterizira kronični tok i poremećaj svih vrsta metabolizma:
- debeo;
- ugljikohidrati;
- proteini;
- voda-sol;
- mineral.
Zanimljivo je da dijabetes ne pogađa samo ljude, već i neke životinje, na primjer, mačke također pate od ove bolesti.
Na bolest se može posumnjati po najupečatljivijim simptomima poliurije (gubitak tečnosti u urinu) i polidipsije (neutoljiva žeđ). Termin "dijabetes" prvi je upotrijebio Demetrios iz Apamanije u 2. vijeku prije nove ere. Riječ u prijevodu s grčkog znači „probijanje“.
To je bila ideja dijabetesa: osoba stalno gubi tekućinu, a zatim je, poput pumpe, neprekidno dopunjuje. Ovo je glavni simptom bolesti.
Visoka koncentracija glukoze
Thomas Willis je 1675. godine pokazao da s povećanim izlučivanjem urina (poliurija), tečnost može imati slatkoću ili može biti potpuno „bez ukusa“. Diabetes insipidus se u to vrijeme nazivao neukusnim.
Ova bolest je uzrokovana ili patološkim poremećajima bubrega (nefrogeni dijabetes) ili oboljenjem hipofize (neurohipofize) i manifestuje se narušavanjem biološkog djelovanja ili lučenjem antidiuretskog hormona.
Drugi naučnik, Metju Dobson, dokazao je svetu da je slatkoća u urinu i krvi dijabetičara posledica visoke koncentracije glukoze u krvotoku. Stari Indijanci su primijetili da slatkoća dijabetičkog urina privlači mrave i dali su toj bolesti naziv "bolest slatkog urina".
Japanski, kineski i korejski ekvivalenti ove fraze zasnovani su na istoj kombinaciji slova i znače istu stvar. Kada su ljudi naučili da mjere koncentraciju šećera ne samo u urinu, već i u krvotoku, odmah su otkrili da šećer prvo raste u krvi. I tek kada njegov nivo u krvi pređe dozvoljeni prag za bubrege (oko 9 mmol/l), šećer se pojavljuje u urinu.
Ideja koja je u osnovi dijabetesa morala se ponovo promijeniti, jer se pokazalo da mehanizam zadržavanja šećera u bubrezima nije narušen. Otuda zaključak: ne postoji nešto kao što je "šećerna inkontinencija".
Međutim, stara paradigma ostala je vezana za novo patološko stanje zvano "bubrežni dijabetes". Glavni uzrok ove bolesti zapravo je bio smanjenje bubrežnog praga šećera u krvi. Kao rezultat toga, pri normalnoj koncentraciji glukoze u krvi, uočena je njena pojava u urinu.
Drugim riječima, kao i kod , pokazalo se da je stari koncept tražen, ali ne za dijabetes, već za sasvim drugu bolest.
Tako je teorija šećerne inkontinencije napuštena u korist drugog koncepta - visoke koncentracije šećera u krvi.
Ova pozicija je danas glavni ideološki alat za postavljanje dijagnoze i procenu efikasnosti lečenja. Istovremeno, savremeni koncept dijabetesa ne zaustavlja se samo na činjenici visokog šećera u krvotoku.
Čak se može sa sigurnošću reći da teorija „visokog šećera u krvi“ završava istoriju naučnih hipoteza o ovoj bolesti, koje se svode na ideje o sadržaju šećera u tečnostima.
Nedostatak insulina
Sada ćemo govoriti o hormonskoj istoriji naučnih izjava o dijabetesu. Prije nego što su naučnici shvatili da nedostatak inzulina u tijelu dovodi do razvoja bolesti, napravili su nekoliko velikih otkrića.
 Oscar Minkowski i Joseph von Mehring predstavili su nauci dokaze 1889. godine da nakon što je psu odstranjen pankreas, životinja pokazuje pune znakove dijabetesa. Drugim riječima, etiologija bolesti direktno ovisi o funkcionalnosti ovog organa.
Oscar Minkowski i Joseph von Mehring predstavili su nauci dokaze 1889. godine da nakon što je psu odstranjen pankreas, životinja pokazuje pune znakove dijabetesa. Drugim riječima, etiologija bolesti direktno ovisi o funkcionalnosti ovog organa.
Drugi naučnik, Edward Albert Sharpay, je 1910. godine iznio hipotezu da patogeneza dijabetes melitusa leži u nedostatku kemikalije koju proizvode Langerhansova otočića smještena u gušterači. Naučnik je ovoj supstanci dao naziv insulin, od latinskog "insula", što znači "ostrvo".
Ovu pretpostavku i endokrinu prirodu pankreasa potvrdila su 1921. još dva naučnika, Charles Herbert Best i Frederick Grant Banting.
Terminologija danas
Savremeni izraz "dijabetes melitus tipa 1" kombinuje dva različita prethodno postojeća koncepta:
- dijabetes ovisan o inzulinu;
- dijabetes u djetinjstvu.
Izraz "dijabetes melitus tipa 2" također sadrži nekoliko zastarjelih pojmova:
- dijabetes neovisan o inzulinu;
- bolest povezana s gojaznošću;
- Dijabetes odraslih.
Međunarodni standardi koriste samo terminologiju “tip 1” i “tip 2”. U nekim izvorima možete pronaći koncept „dijabetesa tipa 3“, što znači:
- trudnice;
- “dvostruki DM” (insulin-rezistentni tip 1 DM);
- Dijabetes tipa 2, koji se razvio prije potrebe za injekcijama inzulina;
- „Dijabetes tipa 1.5” (autoimuni latentni dijabetes kod odraslih).
Klasifikacija bolesti
Dijabetes tipa 1 se prema uzrocima dijeli na idiomatski i autoimuni. Etiologija dijabetesa tipa 2 leži u ekološkim uzrocima. Drugi oblici bolesti mogu biti posljedica:
- Genetski defekt u funkciji insulina.
- Genetska patologija funkcije beta stanica.
- Endokrinopatije.
- Bolesti endokrinog regiona pankreasa.
- Bolest je uzrokovana infekcijama.
- Bolest je uzrokovana upotrebom lijekova.
- Rijetki oblici imunološki posredovanog dijabetesa.
- Nasljedni sindromi koji se kombiniraju sa dijabetes melitusom.
Etiologija gestacijskog dijabetesa, klasifikacija prema komplikacijama:
- Nefropatija.
- Retinopatija.
- Dijabetička polineuropatija.
- Dijabetička makro- i mikroangiopatija.
Formulacija dijagnoze
Prilikom pisanja dijagnoze, doktor na prvo mjesto stavlja tip dijabetesa. Za dijabetes koji nije nezavisan od insulina, pacijentova kartica pokazuje osetljivost pacijenta na oralne hipoglikemijske agense (bez obzira da li postoji rezistencija ili ne).
Drugu poziciju zauzima stanje metabolizma ugljikohidrata, a zatim slijedi lista komplikacija bolesti koje su prisutne kod ovog pacijenta.
Patogeneza
Patogenezu dijabetes melitusa razlikuju dvije glavne točke:
- Nedostatak proizvodnje inzulina stanicama pankreasa.
- Patologija interakcije hormona sa ćelijama tela. Inzulinska rezistencija je posljedica izmijenjene strukture ili smanjenja broja receptora karakterističnih za inzulin, poremećaja unutarćelijskih mehanizama prijenosa signala s receptora na ćelijske organele, promjene u strukturi ćelijskog prijenosa ili samog inzulina.
Dijabetes tipa 1 karakterizira prvi tip oštećenja.
Patogeneza razvoja ove bolesti je masovno uništavanje beta ćelija pankreasa (Langerhansova otočića). Kao rezultat toga, dolazi do kritičnog smanjenja razine inzulina u krvi.
Bilješka! Do smrti velikog broja ćelija pankreasa može doći i usled stresnih stanja, virusnih infekcija i autoimunih bolesti, u kojima ćelije imunog sistema organizma počinju da proizvode antitela protiv beta ćelija.
Ova vrsta dijabetesa tipična je za mlade ljude ispod 40 godina i djecu.
Inzulinski neovisni dijabetes karakteriziraju poremećaji opisani u stavu 2. gore. Kod ovog oblika bolesti inzulin se proizvodi u dovoljnim količinama, ponekad čak i u povećanim količinama.
Međutim, javlja se inzulinska rezistencija (poremećena interakcija tjelesnih stanica s inzulinom), čiji je glavni uzrok disfunkcija membranskih receptora za inzulin kod prekomjerne tjelesne težine (gojaznost).
Gojaznost je glavni faktor rizika za razvoj dijabetesa tipa 2. Receptori, zbog promjena u svom broju i strukturi, gube sposobnost interakcije s inzulinom.
Kod nekih tipova dijabetesa koji ne ovise o inzulinu, struktura samog hormona može biti podvrgnuta patološkim promjenama. Osim gojaznosti, postoje i drugi faktori rizika za ovu bolest:
- loše navike;
- hronično prejedanje;
- starija dob;
- sjedilački način života;
- arterijska hipertenzija.
Možemo reći da ova vrsta dijabetesa često pogađa ljude nakon 40 godina. Ali postoji i nasljedna predispozicija za ovu bolest. Ako dijete ima nekog od svojih rođaka, vjerovatnoća da će beba naslijediti dijabetes tipa 1 je blizu 10%, a dijabetes neovisan o inzulinu može se javiti u 80% slučajeva.
Bitan! Bez obzira na mehanizam razvoja bolesti, kod svih dijabetičara dolazi do trajnog povećanja koncentracije šećera u krvi i metaboličkih poremećaja u tkivima koja postaju nesposobna za hvatanje glukoze iz krvotoka.
Ova patologija dovodi do visokog katabolizma proteina i masti s razvojem ketoacidoze.
Kao rezultat visokog nivoa šećera u krvi dolazi do povećanja osmotskog pritiska, što rezultira velikim gubitkom tečnosti i elektrolita (poliurija). Stalno povećanje koncentracije šećera u krvi negativno utječe na stanje mnogih tkiva i organa, što u konačnici dovodi do razvoja ozbiljnih komplikacija bolesti:
- dijabetičko stopalo;
- nefropatija;
- retinopatija;
- polineuropatija;
- makro- i mikroangiopatija;
- dijabetička koma.
Dijabetičari doživljavaju teške zarazne bolesti i smanjenu imunološku reaktivnost.
Klinički simptomi dijabetesa
Kliničku sliku bolesti izražavaju dvije grupe simptoma – primarni i sekundarni.
Glavni simptomi
Poliurija
Stanje se karakteriše velikim količinama izlučenog urina. Patogeneza ovog fenomena je povećanje osmotskog pritiska tečnosti zbog šećera otopljenog u njoj (normalno ne bi trebalo da bude šećera u urinu).
Polidipsija
Bolesnika muči stalna žeđ, koja je uzrokovana velikim gubicima tekućine i povećanjem osmotskog tlaka u krvotoku.
Polifagija
Konstantna neutaživa glad. Ovaj simptom nastaje kao posljedica metaboličkih poremećaja, tačnije, nemogućnosti stanica da zarobe i razgrade glukozu u odsustvu hormona inzulina.
Gubitak težine
Ova manifestacija je najtipičnija za dijabetes ovisan o inzulinu. Štoviše, gubitak težine javlja se u pozadini povećanja apetita pacijenta.
Gubitak težine, a u nekim slučajevima i iscrpljenost, objašnjava se pojačanim katabolizmom masti i proteina zbog isključenja glukoze iz energetskog metabolizma u stanicama.
Glavni simptomi dijabetesa ovisnog o inzulinu razvijaju se akutno. Pacijenti obično mogu tačno imenovati period ili datum njihovog nastanka.
Manji simptomi
To uključuje niskospecifične kliničke manifestacije koje se razvijaju sporo i tokom dugog vremenskog perioda. Ovi simptomi su tipični za oba tipa dijabetesa:
- glavobolja;
- oštećenje vida;
- svrab sluzokože (vaginalni svrab);
- svrab kože;
- opća slabost mišića;
- upalne lezije kože koje je teško liječiti;
- kod dijabetesa ovisnog o inzulinu, prisutnost acetona u urinu.
Inzulinski ovisan dijabetes (tip 1)
Patogeneza ove bolesti leži u nedovoljnoj proizvodnji inzulina od strane beta ćelija pankreasa. Beta stanice odbijaju obavljati svoju funkciju zbog njihovog uništenja ili utjecaja bilo kojeg patogenog faktora:
- autoimune bolesti;
- stres;
- virusna infekcija.
Dijabetes tipa 1 čini 1-15% svih slučajeva dijabetes melitusa, a najčešće se bolest razvija u djetinjstvu ili adolescenciji. Simptomi ove bolesti brzo napreduju i dovode do raznih teških komplikacija.